题目内容
17.人类的生产生活离不开材料.(1)家用电器制造需用铜导线,这是利用铜具有优良的导电性,要验证镁、铝、铜的活动性顺序,现已选择了打磨过的铝丝,硫酸铜溶液,你认为还需要的溶液是硫酸镁溶液.
(2)CO可作冶金工业原料,但对人体健康有害,写出炼铁高炉中CO还原氧化铁的化学反应方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;煤气中毒是因为CO与血液中血红蛋白结合,造成人体缺氧.
(3)现有一包铜、锌混合粉末,在空气中充分灼烧后,加入稀硫酸至固体恰好溶解,再加入一定量的铁粉,充分反应后过滤,得到滤渣和滤液,则滤渣中一定有铜;滤液中溶质一定有硫酸锌、硫酸亚铁.
分析 (1)根据金属的导电性及金属活动性顺序表的应用分析回答.
(2)根据炼铁的原理及一氧化碳中毒的机理分析回答;
(3)根据金属活动性顺序的内容以及应用分析回答;
解答 解:(1)家用空调常用铜线圈,这是利用铜具有优良的导电性.要验证金属的活动性顺序一般遵循:三取中的原则,即取中间金属的单质和两端金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.所以,要验证镁、铝、铜的活动性顺序,他选择了打磨过的铝丝、硫酸铜溶液,他还需要的溶液是硫酸镁溶液.
(2)高炉炼铁中CO还原氧化铁的化学反应方程式是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;煤气中毒是因为CO与血液中 血红蛋白结合,造成人体缺氧.
(3)取铜、锌混合粉末,在空气中充分灼烧后,生成对应的氧化铜和氧化锌,再加入稀硫酸至固体恰好溶解后,生成对应的硫酸铜和硫酸锌;“再加入一定量的铁粉”时,我们根据“在金属活动性顺序中,位置靠前的金属一般可以将位于其后的金属从它们的盐溶液中置换出来”,可以得知铁能把铜置换出来,而不能把锌置换出来,所以滤渣中一定含有铜;根据铁与硫酸铜溶液反应的化学方程式可以知道反应后生成硫酸亚铁和铜,所以滤液中一定有反应后生成的硫酸亚铁和未参加反应的硫酸锌溶液,
故答为:(1)导电,硫酸镁;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;血红蛋白;(3)铜,硫酸锌和硫酸亚铁.
点评 本题主要考查了金属的活动性顺序的运用,明确金属和酸及金属和盐溶液反应的规律是解决问题的关键;在验证三种金属活动性强弱关系时,通常采取“三取中”的方法:取中间金属的单质或两端金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.

 名校课堂系列答案
名校课堂系列答案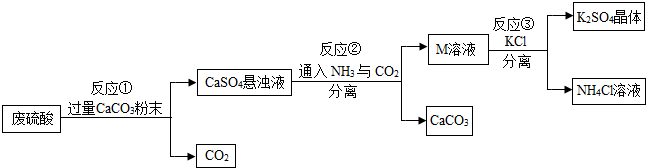
| 物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
| 溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(2)M溶液的溶质主要成分是NH4Cl(填化学式).
(3)洗涤反应③所得晶体不用水面用饱和K2SO4溶液的目的是减少K2SO4的溶解,检验此晶体是否洗涤干净的方法是取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净.
| A. | 茶氨酸中碳、氢元素的质量比为1:2 | |
| B. | 一个茶氨酸分子中含有1个氮分子和1个臭氧分子 | |
| C. | 茶氨酸中氢元素的质量分数最大 | |
| D. | 茶氨酸属于有机化合物 |
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 惰性气体 |

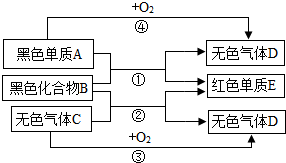 A是非金属,E是金属,B、C、D是化合物,它们之间有如图所示的转化关系(反应条件已略去):
A是非金属,E是金属,B、C、D是化合物,它们之间有如图所示的转化关系(反应条件已略去):