题目内容
2.人类社会的发展离不开常见金属和金属材料,用我们学到的化学知识和方法能分析和解释许多现象.(1)下列生活用品,主要利用金属具有良好导热性的是:A.

(2)常见的三种金属被发现、使用的先后顺序依次为:铜、铁、铝.金属大规模被使用的先后顺序跟下列③(填序号)选项关系最大.
①地壳中金属元素的含量 ②金属的导电性 ③金属活动性
(3)工业上用赤铁矿(主要成份为氧化铁)炼铁的化学反应方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.世界上每年有近四分之一的钢铁被锈蚀,为了保护金属资源我们必须学会防锈,下列介绍的实例只利用隔绝氧气来达到防锈的是:C.

(4)工业生产中,切割铁板时用硫酸铜溶液在铁板上画线可留下红色的印迹.有关反应的化学方程式为Fe+CuSO4═Cu+FeSO4.
(5)铁粉常用作双吸剂,将一包部分变质的双吸剂放入过量稀盐酸中,充分反应后所得溶液中的溶质可能是①FeCl2、HCl②FeCl2、FeCl3和HCl.(友情提示:在溶液中可发生Fe+2FeCl3=3FeCl2反应)
分析 (1)根据常见金属的性质和应用分析判断.
(2)根据冶炼的难易程度与金属活动性的关系回答.
(3)根据一氧化碳还原氧化铁生成铁和二氧化碳写出化学反应式;
(4)根据铁能置换硫酸铜生中铜写出化学反应式;
(5)根据铁及铁的化合物的性质来回答.
解答 解:(1)铸铁饮具主要利用金属具有良好导热性.
(2)金属的活动性越强,越难冶炼,大规模被使用越晚,所以金属大规模被使用的先后顺序跟金属活动性有关.
(3)一氧化碳在高温条件下还原氧化铁生成铁和二氧化碳,化学反应式是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;防锈一般要隔绝氧气和水,但夏天停暖后气片内注满水防止内部生锈,只是隔绝氧气防锈.
(4)铁的活动性大于铜,铁可置换出硫酸铜中铜,留下红色的印迹,化学反应式是:Fe+CuSO4═Cu+FeSO4.
(5)双吸剂变质即有部分铁生锈,投入过量的盐酸中,发生的反应为:Fe+2HCl=FeCl2+H2↑、Fe2O3+6HCl=2FeCl3+3H2O、Fe+2FeCl3=3FeCl2,据反应的可能情况,溶液中一定有氯化亚铁及剩余的盐酸,氯化铁可能存在.
故答案为.(1)A.(2)③.(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2; C.(4)Fe+CuSO4═Cu+FeSO4;(5)①FeCl2、HCl②FeCl2、FeCl3和HCl.
点评 本题考查了铁作为双吸剂的原理以及生锈原理和有关反应的化学方程式的书写问题,完成此题,要熟悉铁锈蚀的条件、常见化学反应式的书写、铁与酸的反应.

练习册系列答案
相关题目
13.如图表示的是KNO3和NaNO3的溶解度曲线,下列说法正确的是( )
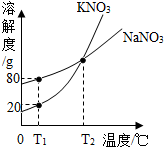

| A. | T2℃时,KNO3溶液的浓度一定等于NaNO3溶液的浓度 | |
| B. | T1℃时,在50g水里加入15g KNO3固体,充分溶解,可得到65g溶液 | |
| C. | T1℃时,往180g NaNO3饱和溶液中加入620g水可配成质量分数为10%的NaNO3溶液 | |
| D. | 若KNO3中混有少量NaNO3,可用蒸发溶剂的方法提纯 |
10.下列有关灭火方法的说法中,错误的是( )
| A. | 清除可燃物 | B. | 降低着火点 | C. | 隔绝空气 | D. | 隔离可燃物 |
7.探究实验
(1)探究物质性质
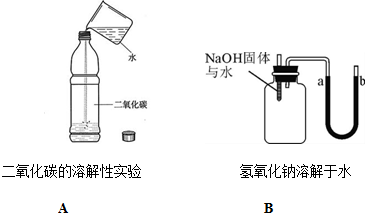
上述A、B两个实验都是通过压强的变化来间接感知.B实验中b(填a或b)处的水位升高的.
(2)探究可燃物燃烧条件
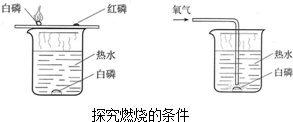
实验中探究可燃物的燃烧条件,它是通过控制可燃物是否与氧气接触和控制可燃物温度是否达到着火点来探究可燃物燃烧的条件.能证明燃烧必须与氧气接触的实验现象是A实验中水下的白磷不燃烧而铜片上的白磷燃烧;采用了对比的实验手段
(3)物质性质的应用:
(1)探究物质性质

上述A、B两个实验都是通过压强的变化来间接感知.B实验中b(填a或b)处的水位升高的.
(2)探究可燃物燃烧条件

实验中探究可燃物的燃烧条件,它是通过控制可燃物是否与氧气接触和控制可燃物温度是否达到着火点来探究可燃物燃烧的条件.能证明燃烧必须与氧气接触的实验现象是A实验中水下的白磷不燃烧而铜片上的白磷燃烧;采用了对比的实验手段
(3)物质性质的应用:
| 实验序号 | 实验目的 | 实验方案 | 实验现象 | 结论 |
实验1 | 检验草木灰中是否含碳酸盐 |  | 有气泡冒出,澄清石灰水变浑浊 | 草木灰的主要成分是碳酸钾 |
14.下列实验方案中,实验操作合理的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 验证二氧化碳能与水反应生成碳酸 | 向收集满二氧化碳的集气瓶中加入约$\frac{1}{3}$体积的滴有酚酞的水,振荡 |
| B | 检验氢氧化钠溶液已部分变质 | 取少量溶液,滴加足量的氯化钡溶液,过滤,向滤液中滴加酚酞溶液 |
| C | 探究稀硫酸与氢氧化钠溶液是否完全反应 | 向反应后所得的溶液中滴加硝酸银溶液 |
| D | 除去CO2中的SO2气体和水蒸气 | 将混合气体依次通过NaOH溶液和浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
12.下列物质中,属于化合物的是( )
| A. | 水 | B. | 黄铜 | C. | 空气 | D. | 白磷 |