题目内容
19.用化学方程式回答:(1)向紫色石蕊试液中通二氧化碳,溶液变红CO2+H2O═H2CO3
(2)加热(1)中溶液,溶液又由红色变为紫色H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑
(3)向澄清石灰水中通二氧化碳,溶液变浑浊CO2+Ca(OH)2═CaCO3↓+H2O.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)二氧化碳与水反应生成碳酸,碳酸使紫色石蕊试液变红,反应的化学方程式为:CO2+H2O═H2CO3.故填:CO2+H2O═H2CO3;
(2)碳酸不稳定,在加热条件下生成水和二氧化碳,溶液又由红色变为紫色,反应的化学方程式为:H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑.故填:H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑;
(3)石灰水中的溶质是氢氧化钙,能与二氧化碳反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.故填:CO2+Ca(OH)2═CaCO3↓+H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
10.能源和环境已经成为人们日益关注的问题.
(1)目前利用最多的是煤、石油和天然气等化石燃料,煤燃烧会产生大量的二氧化碳、二氧化硫和一氧化碳等气体,其中SO2(填化学式)溶于水会导致酸雨.
(2)氢气作为一种清洁燃料没有大规模使用的原因是AB.
A.氢气的贮存困难 B.获得氢气的成本高 C.制备氢气的原料偏少 D.氢气燃烧的热值不高
(3)氢气作燃料有无毒、热值高、无污染等优点.在催化剂、光照条件下,水分解得到氢能源,该方法的化学方程式为:2H2O$\frac{\underline{太阳能}}{催化剂}$2H2↑+O2↑.
(4)为解决化石能源面临枯竭和环保问题而利用了新能源的是AB.
A.风力发电 B.太阳能飞机 C.海上采油
(5)奥运会火炬使用的燃料为A物质,纯净物A物质在B物质中充分燃烧,发生反应 A+5B$\frac{\underline{\;点燃\;}}{\;}$3C+4D (微观示意图如表所示).
①上述化学反应中提供氧,具有氧化性的物质是O2(填化学式);
②A物质所含各元素间的质量比为9:2.
(1)目前利用最多的是煤、石油和天然气等化石燃料,煤燃烧会产生大量的二氧化碳、二氧化硫和一氧化碳等气体,其中SO2(填化学式)溶于水会导致酸雨.
(2)氢气作为一种清洁燃料没有大规模使用的原因是AB.
A.氢气的贮存困难 B.获得氢气的成本高 C.制备氢气的原料偏少 D.氢气燃烧的热值不高
(3)氢气作燃料有无毒、热值高、无污染等优点.在催化剂、光照条件下,水分解得到氢能源,该方法的化学方程式为:2H2O$\frac{\underline{太阳能}}{催化剂}$2H2↑+O2↑.
(4)为解决化石能源面临枯竭和环保问题而利用了新能源的是AB.
A.风力发电 B.太阳能飞机 C.海上采油
(5)奥运会火炬使用的燃料为A物质,纯净物A物质在B物质中充分燃烧,发生反应 A+5B$\frac{\underline{\;点燃\;}}{\;}$3C+4D (微观示意图如表所示).
| 物质 | A | B | C | D |  |
| 分子示意图 | ? |  |  |  |
②A物质所含各元素间的质量比为9:2.
14.某化学兴趣活动小组的同学作了以下两个探究实验:
(1)探究影响化学反应速率的因素:在实验室制取二氧化碳的研究中,进行了如下实验:
①实验室制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应速率的影响,可选择实验甲与实验乙(选填实验编号)进行对照实验.
③若要研究反应物的接触面积对反应速率的影响,可选择实验甲与实验丙(选填实验编号)进行对照实验.
④化学反应的实质是微观粒子相互接触、碰撞的结果,试从微观角度解释“反应物的接触面积越大,化学反应速率越快”的原因是:反应物浓度越大,单位体积的反应物中含有的粒子数越多,粒子间碰撞的概率越大,化学反应速率越快.
⑤乙和丁相比较,产生气体的速率较快的是丁,完全反应后,产生二氧化碳的质量相等(填“相等”或“不等”).
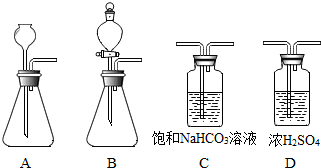
⑥若要选择了这组药品制取二氧化碳,为了能得到较平稳的气流,应选择如图装置中的B(填“A”或“B”),理由是分液漏斗可以控制盐酸加入的速率,从而控制反应的速率.由于浓盐酸具有强烈的挥发性,会导致收集到的二氧化碳中含有氯化氢气体,为了得到干燥、纯净的二氧化碳,可将产生的二氧化碳依次通过下列装置C、D.(温馨提示:①浓硫酸具有吸水性,可作干燥剂;②二氧化碳不与饱和NaHCO3溶液反应,氯化氢可与之反应,相应的化学方程式:NaHCO3+HCl═NaCl+H2O+CO2↑)
(2)探究二氧化碳与氢氧化钠的反应.
通过查阅资料可知:①氢氧化钠与氢氧化钙的化学性质相似,其水溶液也能与二氧化碳反应.②通常情况下,1体积水能溶解1体积二氧化碳.
二氧化碳通入澄清石灰水,石灰水变浑浊,相应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O,某同学将二氧化碳通入氢氧化钠溶液,无明显现象,模仿二氧化碳与氢氧化钙反应的化学方程式,写出二氧化碳与氢氧化钠反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
对于无明显现象的化学反应,可通过验证反应物的减少或生成物的存在来证明发生了化学反应,某同学根据这个原则设计了三个实验方案验证二氧化碳确与氢氧化钠溶液发生了化学反应.
其中方案二(写出方案编号)不能证明二氧化碳确与氢氧化钠反应了,理由是二氧化碳能够溶于水,导致塑料瓶中压强减小,从而导致塑料瓶变瘪.
| 试液编号药品 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
①实验室制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应速率的影响,可选择实验甲与实验乙(选填实验编号)进行对照实验.
③若要研究反应物的接触面积对反应速率的影响,可选择实验甲与实验丙(选填实验编号)进行对照实验.
④化学反应的实质是微观粒子相互接触、碰撞的结果,试从微观角度解释“反应物的接触面积越大,化学反应速率越快”的原因是:反应物浓度越大,单位体积的反应物中含有的粒子数越多,粒子间碰撞的概率越大,化学反应速率越快.
⑤乙和丁相比较,产生气体的速率较快的是丁,完全反应后,产生二氧化碳的质量相等(填“相等”或“不等”).
⑥若要选择了这组药品制取二氧化碳,为了能得到较平稳的气流,应选择如图装置中的B(填“A”或“B”),理由是分液漏斗可以控制盐酸加入的速率,从而控制反应的速率.由于浓盐酸具有强烈的挥发性,会导致收集到的二氧化碳中含有氯化氢气体,为了得到干燥、纯净的二氧化碳,可将产生的二氧化碳依次通过下列装置C、D.(温馨提示:①浓硫酸具有吸水性,可作干燥剂;②二氧化碳不与饱和NaHCO3溶液反应,氯化氢可与之反应,相应的化学方程式:NaHCO3+HCl═NaCl+H2O+CO2↑)

(2)探究二氧化碳与氢氧化钠的反应.
通过查阅资料可知:①氢氧化钠与氢氧化钙的化学性质相似,其水溶液也能与二氧化碳反应.②通常情况下,1体积水能溶解1体积二氧化碳.
二氧化碳通入澄清石灰水,石灰水变浑浊,相应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O,某同学将二氧化碳通入氢氧化钠溶液,无明显现象,模仿二氧化碳与氢氧化钙反应的化学方程式,写出二氧化碳与氢氧化钠反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
对于无明显现象的化学反应,可通过验证反应物的减少或生成物的存在来证明发生了化学反应,某同学根据这个原则设计了三个实验方案验证二氧化碳确与氢氧化钠溶液发生了化学反应.
| 方案编号 | 方案 | 实验现象 | 结论 |
| 一 | 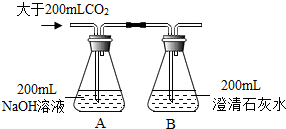 | A、B瓶均无明显现象 | 二氧化碳确与氢氧化钠反应了 |
| 二 | 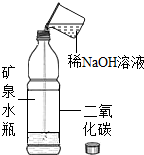 加入NaOH溶液后,盖好瓶盖,振荡 | 塑料瓶变瘪 | 二氧化碳确与氢氧化钠反应了 |
| 三 | 往二氧化碳和氢氧化钠溶液作用后的液体中加入稀盐酸 | 有气泡产生 | 二氧化碳确与氢氧化钠反应了 |
8.下列各组物质里,前者是后者的溶质的是( )
| A. | 生石灰、石灰水 | B. | 酒精、碘酒 | ||
| C. | 氯化氢、盐酸 | D. | 二氧化碳、碳酸溶液 |
