题目内容
5.根据下面所示的实验回答问题:
(1)甲实验通过量筒中的水的体积变化测出氧气的体积;写出红磷燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)将一个充满二氧化碳的试管倒立在盛有澄清石灰水的烧杯中,可以观察到的现象是试管内的石灰水变浑浊;试管内液面上升;该反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O.
(3)丙是木炭在氧气中燃烧的实验,木炭在氧气里燃烧比在空气里燃烧更剧烈,原因是纯氧中氧气浓度高于空气中氧气的浓度.
分析 (1)通过水的体积变化可以测定试剂瓶中氧气的含量,根据磷燃烧的反应写出反应的化学方程式;
(2)二氧化碳能与澄清石灰水反应生成碳酸钙沉淀和水,反应会使气体减少,造成试管内压强减小,液体进入试管;
(3)根据可燃物燃烧时的不同现象与氧气的接触面积;氧气的浓度;可燃物的性质有关进行分析.
解答 解:(1)A实验通过量筒中水的体积变化测出氧气的体积;磷与氧气反应生成五氧化二磷;故填:水的体积;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)二氧化碳能与氢氧化钙反应生成碳酸钙沉淀,导致试管内的溶液变浑浊,二氧化碳参与反应导致试管内的压强变小,液面会上升;二氧化碳与氢氧化钙反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O.
故答案为:试管内的石灰水变浑浊;试管内液面上升;CO2+Ca(OH)2═CaCO3↓+H2O.
(3)可燃物燃烧时的不同现象与氧气的接触面积;氧气的浓度;可燃物的性质 有关;木炭在氧气中燃烧比在空气中燃烧更剧烈的原因是氧气浓度大,空气中氧气浓度小.故填:纯氧中氧气浓度高于空气中氧气的浓度.
点评 本题主要考查实验现象、氧气体积的测定、二氧化碳的性质以及化学方程式的书写等方面的知识,解答时应该分析实验现象,要根据质量守恒定律书写化学方程式.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
14.某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究.
【提出问题】
这包干燥剂是否变质,成分是什么?
【猜想假设】
猜想一:全部是CaO;
猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2;
猜想四:是Ca(OH)2和CaCO3的混合物.
【实验探究】
(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含CaO.
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有CaCO3.
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下三种方案.
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中.请你参与实验,并填写表中的空白:
写出方案二发生的化学反应方程式:Ca(OH)2+CO2═CaCO3↓+H2O.
【实验结论】
通过以上实验探究,得出猜想四成立.
【拓展迁移】
小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注密封保存.
【提出问题】
这包干燥剂是否变质,成分是什么?
【猜想假设】
猜想一:全部是CaO;
猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2;
猜想四:是Ca(OH)2和CaCO3的混合物.
【实验探究】
(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含CaO.
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有CaCO3.
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下三种方案.
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中.请你参与实验,并填写表中的空白:
| 实验方案 | 方案一 | 方案二 | 方案三 |
| 实验操作 | 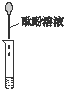 | 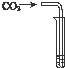 | 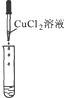 |
| 实验现象 | 溶液由无色变红色 | 澄清溶液变浑浊 | 产生蓝色絮状沉淀 |
【实验结论】
通过以上实验探究,得出猜想四成立.
【拓展迁移】
小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注密封保存.
15.合肥某校研究性学习活动小组的同学利用课余时间调查雾霾产生的原因,提出了一些减少雾霾的建议,其中正确的是( )
| A. | 鼓励开私家车 | B. | 鼓励燃煤发电 | ||
| C. | 鼓励使用太阳能热水器 | D. | 鼓励露天焚烧垃圾 |
 建知识网络是一种重要的学习方法,如图是氧气和部分物质间的转化关系,请回答.(提升:“-”表示两物质间互相反应,“→”表示由某物质可转化为另一物质).
建知识网络是一种重要的学习方法,如图是氧气和部分物质间的转化关系,请回答.(提升:“-”表示两物质间互相反应,“→”表示由某物质可转化为另一物质).

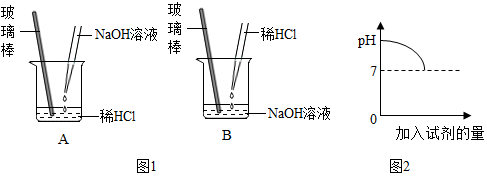
 小雪在实验室做酸和碱与指示剂反应的实验,所用试剂如图所示,实验后把废液集中倒入废液缸中.
小雪在实验室做酸和碱与指示剂反应的实验,所用试剂如图所示,实验后把废液集中倒入废液缸中.