题目内容
天平两边各放质量相等的烧杯,分别盛有100克溶质质量分数为9.8%的稀硫酸,此时 天平平衡.若将
下列各组的两种物质分别加入左右两烧杯中,充分反应后,天平仍平衡的是( )
下列各组的两种物质分别加入左右两烧杯中,充分反应后,天平仍平衡的是( )
| A、铜8克,氧化铜8克 |
| B、氯化钡溶液10克,氢氧化镁5克 |
| C、氧化铜4克,碳酸镁8.4克 |
| D、铁5克,铝5克 |
考点:酸的化学性质,根据化学反应方程式的计算
专题:常见的酸 酸的通性
分析:如果酸过量金属完全反应,则相同质量的不同金属与同质量的酸反应后生成气体的质量肯定不同,天平不能保持平衡;如果金属过量酸完全反应,产生H2的质量必相同,此时天平必保持平衡,可以据此求算出生成等质量的氢气所消耗的金属的质量,然后进行判断即可
解答:A、铜与硫酸不反应,加入8g,就增重8g,氧化铜与硫酸反应生成硫酸铜和水,质量也增重8g,天平平衡,故A正确;
B、氯化钡与硫酸反应生成硫酸钡和盐酸,所以加入10g氯化钡就增重10g,氢氧化镁与硫酸反应生成硫酸镁和水,加入5g就增重5g,天平不再平衡,故B错误;
C、氧化铜与硫酸反应生成硫酸铜和水,加入4g质量也增重4g;碳酸镁与硫酸反应生成硫酸镁、水和二氧化碳,8.4g碳酸镁与硫酸反应生成4.4g二氧化碳,所以增重的质量为:8.4g-4.4g=4g,天平平衡,故C正确;
D、铁和铝加入的质量都是5g,与硫酸反应生成氢气不同,铝与硫酸反应产生的氢气多,所以天平偏向加入铁的一边,故D错.
故选AC.
B、氯化钡与硫酸反应生成硫酸钡和盐酸,所以加入10g氯化钡就增重10g,氢氧化镁与硫酸反应生成硫酸镁和水,加入5g就增重5g,天平不再平衡,故B错误;
C、氧化铜与硫酸反应生成硫酸铜和水,加入4g质量也增重4g;碳酸镁与硫酸反应生成硫酸镁、水和二氧化碳,8.4g碳酸镁与硫酸反应生成4.4g二氧化碳,所以增重的质量为:8.4g-4.4g=4g,天平平衡,故C正确;
D、铁和铝加入的质量都是5g,与硫酸反应生成氢气不同,铝与硫酸反应产生的氢气多,所以天平偏向加入铁的一边,故D错.
故选AC.
点评:解决天平平衡题或是天平偏向问题,主要就是比较反应前后烧杯中剩余物质的质量变化量,因为计算的是反应后烧杯中物质的总质量变化,所以常用查量法进行比较.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
下列关于溶液的pH说法,正确的是( )
| A、氢氧化钠溶液加水后,pH降低 |
| B、用pH试纸检验溶液的酸碱度时,先用水湿润试纸 |
| C、在pH=2的盐酸中加入pH=3的盐酸,溶液酸性增强 |
| D、酸和碱混合后,溶液的pH一定等于7 |
 在杠杆的两端分别挂着质量和体积都相同的铁球和铝球,这时杠杆平衡.将两球分别浸泡在质量相同、溶质质量分数也相同的稀硫酸中,如图所示,直至两个烧杯中均没有气泡产生为止,两球的外形变化不大,且无孔洞出现,下列推测中正确的是( )
在杠杆的两端分别挂着质量和体积都相同的铁球和铝球,这时杠杆平衡.将两球分别浸泡在质量相同、溶质质量分数也相同的稀硫酸中,如图所示,直至两个烧杯中均没有气泡产生为止,两球的外形变化不大,且无孔洞出现,下列推测中正确的是( )| A、铝球一定是空心的 |
| B、拿掉烧杯后,杠杆仍然平衡(金属球上附着的液体忽略不计,下同) |
| C、拿掉烧杯后,要想使杠杆平衡,支点应向N移动 |
| D、拿掉烧杯后,要想使杠杆平衡,支点应向M移动 |
如图所示试管的试管口朝向不同可完成不同实验,下列说法错误的是( )
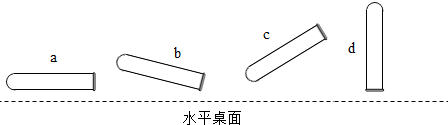

| A、a可用于往试管中添加固体药品 |
| B、b可用于给试管中固体药品加热 |
| C、c可用于给试管中的液体药品加热 |
| D、d可用于排空气法收集少量密度比空气大的气体 |