题目内容
某化学实验室有一瓶黑色固体粉末X(X是纯净物),因试剂瓶标签破损无法确定其成分及有关性质.为此小军进行了以下探究.
Ⅰ探究X的成分
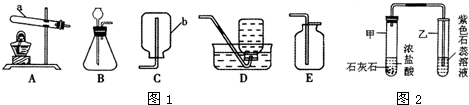
取两份等量的X样品,分别进行如图1所示的实验:
Ⅱ探究X与稀硫酸的反应
稀硫酸中含有H2O、H+、SO42-等粒子,小军分析“实验一、二”后认为:可能是稀硫酸中的H+或SO42-使X溶解.为确定稀硫酸中何种粒子使X溶解,他继续设计了如图所示的实验进行探究:

(1)从“实验一”小军得出X的物理性质是 ;从“实验二”小军推断出X的化学式是 .
(2)“实验三”中的A可能是 (填化学式,下同).“实验四”中的B可能是 .
(3)小军通过上述实验证明稀硫酸中 (填离子符号)才能使X溶解.
Ⅰ探究X的成分
取两份等量的X样品,分别进行如图1所示的实验:
Ⅱ探究X与稀硫酸的反应
稀硫酸中含有H2O、H+、SO42-等粒子,小军分析“实验一、二”后认为:可能是稀硫酸中的H+或SO42-使X溶解.为确定稀硫酸中何种粒子使X溶解,他继续设计了如图所示的实验进行探究:

(1)从“实验一”小军得出X的物理性质是
(2)“实验三”中的A可能是
(3)小军通过上述实验证明稀硫酸中
考点:缺失标签的药品成分的探究,物质的溶解性及影响溶解性的因素,酸的化学性质
专题:科学探究
分析:(1)根据“实验一”的现象判断X的物理性质,根据“实验二”的现象判断推断出X的化学式;
(2)根据固定变量法探究物质的性质的方法分析加入的物质;
(3)根据上述探究,总结能使X溶解的粒子
(2)根据固定变量法探究物质的性质的方法分析加入的物质;
(3)根据上述探究,总结能使X溶解的粒子
解答:解:(1)从“实验一”可知,得出X的物理性质是X难溶于水;由“实验二”知,X与稀硫酸反应生成蓝色物质,即生成硫酸铜,加入铁丝生成了红色的物质为铜,由此可推出X是氧化铜,化学式是:CuO;
(2)通过实验一可知,水分子不能使X溶解,如果要验证H+或SO42-使X溶解,应该考虑单独含有H+或SO42-的物质与CuO反应,观察CuO是否溶解.由“实验三”知,加入A物质与X不反应,所以实验Ⅲ中应加入的物质可以是硫酸钠等可溶性硫酸盐;“实验四”能溶解CuO,所以B物质可能是硫酸或盐酸等酸类物质.所以,
“实验三”中的A可能是Na2SO4.“实验四”中的B可能是HCl.
(3)综合以上分析可知,稀硫酸中H+ 才能使X溶解.
故答为:(1)X难溶于水,CuO;(2)Na2SO4,HCl;(3)H+.
(2)通过实验一可知,水分子不能使X溶解,如果要验证H+或SO42-使X溶解,应该考虑单独含有H+或SO42-的物质与CuO反应,观察CuO是否溶解.由“实验三”知,加入A物质与X不反应,所以实验Ⅲ中应加入的物质可以是硫酸钠等可溶性硫酸盐;“实验四”能溶解CuO,所以B物质可能是硫酸或盐酸等酸类物质.所以,
“实验三”中的A可能是Na2SO4.“实验四”中的B可能是HCl.
(3)综合以上分析可知,稀硫酸中H+ 才能使X溶解.
故答为:(1)X难溶于水,CuO;(2)Na2SO4,HCl;(3)H+.
点评:本题考查了如何探究物质的性质和变化规律,掌握猜想和实验验证的方法.

练习册系列答案
相关题目
水是人类生活不可缺少的物质.下列有关水的叙述不正确的是( )
| A、水是由氢元素和氧元素组成的 |
| B、氢气燃烧生成水和电解水都属于分解反应 |
| C、用肥皂水可以区分硬水和软水 |
| D、根据水的化学式可知,一个水分子中含有两个氢原子和一个氧原子 |