题目内容
6.将一定量的镁放入Cu(NO3)2和AgNO3溶液中,充分反应后过滤,得到滤渣和滤液,分析滤渣和滤液成分.分析 根据在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,金属银、铜、镁的活动性由强到弱的顺序镁>铜>银,当把镁加入到AgNO3和Cu(NO3)2的混合溶液中,首先置换出银,银被置换完才继续置换铜,据此分析.
解答 解:AgNO3、Cu(NO3)2的混合溶液中加入一定量的镁粉,镁能与硝酸银反应生成硝酸镁和银,能与硝酸铜反应生成硝酸镁和铜,铜能与硝酸银反应生成硝酸铜和银,所以镁先与硝酸银反应后再与硝酸铜反应,当镁过量时,滤渣中含有银、铜、镁,滤液成分是硝酸镁;当镁不足或恰好完全反应时,滤渣中一定含有银,可能含有铜;滤液中一定含有的溶质是硝酸锌.
故答案为:当镁过量时,滤渣中含有银、铜、镁,滤液成分是硝酸镁;当镁不足或恰好完全反应时,滤渣中一定含有银,可能含有铜;滤液中一定含有的溶质是硝酸锌.
点评 本题考查了金属活动性顺序的应用,金属放入盐的混合溶液中,首先把活动性最弱的金属置换出来,置换的先后顺序为由弱到强,最强的最后置换出来.

练习册系列答案
相关题目
14.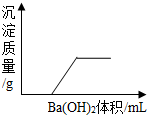 有一溶液是由盐酸、硫酸、硫酸铁、氯化钡、硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )
有一溶液是由盐酸、硫酸、硫酸铁、氯化钡、硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )
 有一溶液是由盐酸、硫酸、硫酸铁、氯化钡、硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )
有一溶液是由盐酸、硫酸、硫酸铁、氯化钡、硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )| A. | 硝酸、氯化铁 | B. | 硫酸、氯化钡 | C. | 盐酸、硝酸铁 | D. | 盐酸、硫酸铁 |
2.下列说法正确的是( )
| A. | 缓慢氧化放出的热量比剧烈氧化放出的热量缓慢 | |
| B. | 对试管内的液体进行加热时,试管口应略向下倾斜 | |
| C. | 分子可以再分,原子不能再分 | |
| D. | 原子不能保持物质的化学性质 |
19. 如图是某化学实验小组验证空气中的氧气含量的装置图.
如图是某化学实验小组验证空气中的氧气含量的装置图.
(1)写出图中红磷燃烧的文字表达式磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)实验测定数据如表:(集气瓶的容积为100mL).
分析实验数据,第2,3,4,6组验证出氧气约占空气体积的$\frac{1}{5}$,第5组出现较大偏差的原因可能是没有冷却到室温读数等(合理即可).
 如图是某化学实验小组验证空气中的氧气含量的装置图.
如图是某化学实验小组验证空气中的氧气含量的装置图.(1)写出图中红磷燃烧的文字表达式磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)实验测定数据如表:(集气瓶的容积为100mL).
| 组别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积/mL | 30 | 21 | 19 | 22 | 15 | 20 |