题目内容
9.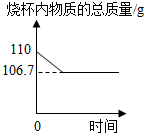 某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取10g放于盛有100g稀盐酸的烧杯中(杂质不溶于水,也不与稀盐酸反应,也不分解),恰好完全反应.测得烧杯内物质的总质量与时间的关系如图所示(气体溶解忽略不计).计算:
某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取10g放于盛有100g稀盐酸的烧杯中(杂质不溶于水,也不与稀盐酸反应,也不分解),恰好完全反应.测得烧杯内物质的总质量与时间的关系如图所示(气体溶解忽略不计).计算:(1)生成二氧化碳的质量是3.3g;
(2)参加反应的碳酸钙的质量是多少?
(3)稀盐酸的质量分数是多少?
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算碳酸钙和HCl的质量,进而求算对应的质量分数.
解答 解:
根据质量守恒定律,二氧化碳的质量为:100g+10g-106.7g=3.3g
设该石灰石样品中碳酸钙的质量为x,稀盐酸中溶质的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x y 3.3g
$\frac{100}{x}$=$\frac{73}{y}$=$\frac{44}{3.3g}$
x=7.5g
y=5.475g
稀盐酸的质量分数为$\frac{5.475g}{100g}$×100%=5.475%
答:(1)生成二氧化碳的质量是 3.3g;
(2)参加反应的碳酸钙的质量是7.5g;
(3)稀盐酸的质量分数是5.475%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.如图是某个化学反应的微观模拟示意图.从图中获得的有关信息不正确的是( )


| A. | 两种参加反应的物质都属于单质 | B. | 该反应为化合反应 | ||
| C. | 化学反应中分子可分为原子 | D. | 生成的物质不可能属于氧化物 |
14.下列典故中,从物质变化的角度分析,主要体现物理变化的是( )
| A. | 水滴石穿 | B. | 野火烧不尽,春风吹又生 | ||
| C. | 春蚕到死丝方尽,蜡炬成灰泪始干 | D. | 爆竹声中一岁除,春风送暖入屠苏 |
18.下列实验基本操作不正确的是( )
| A. |  检验二氧化碳气体 | B. |  吸取和滴加少量液体 | ||
| C. |  取用粉末状固体药品 | D. |  点燃和熄灭酒精灯 |
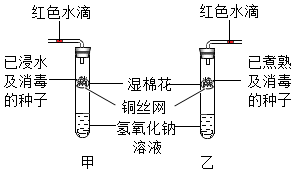 如图是小柯探究种子呼吸作用的实验装置.
如图是小柯探究种子呼吸作用的实验装置. A、B、C、D、E、F、G、H八种物质,有下图所示关系,“→”表示可以向箭头所指方向转化,通常情况下F是一种无色液体,G是一种黑色固体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变.
A、B、C、D、E、F、G、H八种物质,有下图所示关系,“→”表示可以向箭头所指方向转化,通常情况下F是一种无色液体,G是一种黑色固体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变.