题目内容
2.现有H、O、S、C等四种元素,请选择其中一种或几种元素填写符合要求的化学式:①引起酸雨的气体SO2;
②生命活动中不可缺少的气体O2;
③生物体中含量最多的物质H2O;
④导致温室效应的气体CO2.
分析 用所给元素书写物质的化学式时,首先要确定物质的化学名称,然后按照书写化学式的方法、步骤正确的写出物质的化学式.
解答 解:①二氧化硫是引起酸雨的主要物质,其化学式为:SO2;
②人的生命活动离不开呼吸,氧气供给呼吸,故生命活动中不可缺少的气体是氧气,其化学式为:O2;
③生物体中含量最多的物质是水,其化学式为:H2O;
④二氧化碳是导致温室效应的气体,其化学式为:CO2;
故答案为①SO2,②O2,③H2O,④CO2
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
10.某实验小组利用废硫酸液制备K2SO4,设计的流程如下图所示:
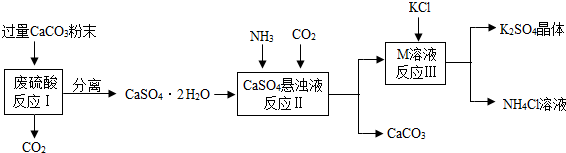
(1)反应II的化学方程式为:CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH4)2SO4:
(2)上述流程中可循环使用的物质有:CaCO3、CO2(填写化学式);
(3)反应Ⅲ中相关物质的溶解度如下表所示:
则反应Ⅲ的化学方程式为:(NH4)2SO4+2KCl=2NH4Cl+K2SO4↓,该反应在常温下能发生的原因是:硫酸钾的溶解度最小;
(4)用饱和K2SO4溶液洗涤反应Ⅲ所得K2SO4晶体的目的主要有两个,一是为了除去K2SO4晶体表面附着的NH4+、Cl-等杂质离子,二是为了减少用水洗涤时K2SO4晶体因溶解而造成的损失.

(1)反应II的化学方程式为:CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH4)2SO4:
(2)上述流程中可循环使用的物质有:CaCO3、CO2(填写化学式);
(3)反应Ⅲ中相关物质的溶解度如下表所示:
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)用饱和K2SO4溶液洗涤反应Ⅲ所得K2SO4晶体的目的主要有两个,一是为了除去K2SO4晶体表面附着的NH4+、Cl-等杂质离子,二是为了减少用水洗涤时K2SO4晶体因溶解而造成的损失.
7.下列现象中,能说明分子不停地做无规则运动的是( )
| A. | 细雨飘飘 | B. | 桂花飘香 | C. | 雪花飞舞 | D. | 树叶飘落 |
14.人类社会的发展离不开能源.当今社会人类利用的能源主要来自化石燃料.回答下列问题:
(1)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属于物理变化,化石燃料中主要含有碳、氢元素,它完全燃烧的产物是二氧化碳和水,此外还含有硫、氮等元素,它们燃烧时会转化为二氧化硫和氮氧化物,造成空气污染.
(2)我国煤炭资源丰富,煤的综合利用措施主要有煤的气化、焦化和液化,在煤的综合利用中,改变煤的组成和结构的过程属于化学变化.
(3)城市居民生活用燃料主要有液化石油气、天然气和煤气,下表是几种气体燃料的价格和热值:
综合考虑以上因素,你将选用哪种燃料?天然气;理由是天然气的热值高,价格相对较低,对环境污染较小.
(1)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属于物理变化,化石燃料中主要含有碳、氢元素,它完全燃烧的产物是二氧化碳和水,此外还含有硫、氮等元素,它们燃烧时会转化为二氧化硫和氮氧化物,造成空气污染.
(2)我国煤炭资源丰富,煤的综合利用措施主要有煤的气化、焦化和液化,在煤的综合利用中,改变煤的组成和结构的过程属于化学变化.
(3)城市居民生活用燃料主要有液化石油气、天然气和煤气,下表是几种气体燃料的价格和热值:
| 燃料名称 | 煤气 | 液化石油气 | 天然气 |
| 价格 | 4.2元/千克 | 8.4元/千克 | 4.8元/千克 |
| 热值 | 1.56×104kJ/kg | 4.5×104kJ/kg | 3.9×104kJ/kg |
11.下列实验操作中错误的是( )
| A. |  闻气味方法 | B. |  滴管用后不洗涤直接放回原瓶 | ||
| C. |  稀释浓硫酸 | D. |  称量氢氧化钠质量 |
12.某食品包装中充有某种气体如图1.实验小组的同学想对该气体的主要成分进行研究.
猜想:甲同学认为可能为氮气,乙同学认为可能为二氧化碳,丙同学认为是氮气和二氧化碳的混合物.
为了进一步研究该气体成分,实验小组的同学进行了如下的探究:
探究一:
探究二:用图2装置继续进行实验(假设每步都完全反应):
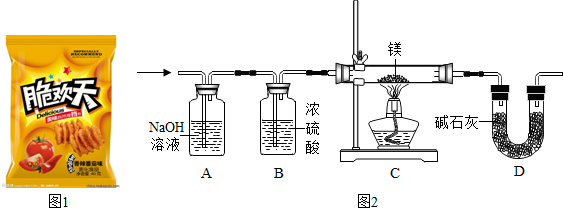 (1)点燃酒精灯前先通一会儿该气体,其作用是赶出装置内的空气,B装置中浓硫酸的作用是除去气体中的水蒸气,C装置中产生的一种淡黄色的固体为氮化镁(Mg3N2),发生反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
(1)点燃酒精灯前先通一会儿该气体,其作用是赶出装置内的空气,B装置中浓硫酸的作用是除去气体中的水蒸气,C装置中产生的一种淡黄色的固体为氮化镁(Mg3N2),发生反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
(2)同学们将C装置中淡黄色固体取出,加入水中,产生一种不溶性碱和能使湿润的红色石蕊试纸变为蓝色的气体,则氮化镁与水反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.通过以上实验探究可以得出:该气体组成为N2和CO2.
猜想:甲同学认为可能为氮气,乙同学认为可能为二氧化碳,丙同学认为是氮气和二氧化碳的混合物.
为了进一步研究该气体成分,实验小组的同学进行了如下的探究:
探究一:
| 实验操作 | 实验现象 | 实验结论 |
| 把气体通入澄清的石灰水溶液中. | 产生白色沉淀 | 甲同学的猜想不正确,该过程中发生反应的方程式为:Ca(OH)2+CO2=CaCO3↓+H2O. |
 (1)点燃酒精灯前先通一会儿该气体,其作用是赶出装置内的空气,B装置中浓硫酸的作用是除去气体中的水蒸气,C装置中产生的一种淡黄色的固体为氮化镁(Mg3N2),发生反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
(1)点燃酒精灯前先通一会儿该气体,其作用是赶出装置内的空气,B装置中浓硫酸的作用是除去气体中的水蒸气,C装置中产生的一种淡黄色的固体为氮化镁(Mg3N2),发生反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.(2)同学们将C装置中淡黄色固体取出,加入水中,产生一种不溶性碱和能使湿润的红色石蕊试纸变为蓝色的气体,则氮化镁与水反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.通过以上实验探究可以得出:该气体组成为N2和CO2.