题目内容
10.某实验小组利用废硫酸液制备K2SO4,设计的流程如下图所示: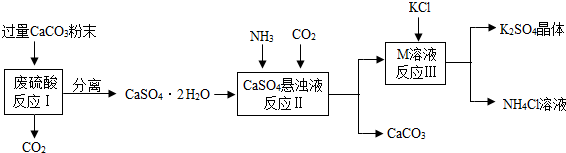
(1)反应II的化学方程式为:CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH4)2SO4:
(2)上述流程中可循环使用的物质有:CaCO3、CO2(填写化学式);
(3)反应Ⅲ中相关物质的溶解度如下表所示:
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)用饱和K2SO4溶液洗涤反应Ⅲ所得K2SO4晶体的目的主要有两个,一是为了除去K2SO4晶体表面附着的NH4+、Cl-等杂质离子,二是为了减少用水洗涤时K2SO4晶体因溶解而造成的损失.
分析 根据反应物和生成物书写反应的化学方程式;根据可以循环利用的物质解答;根据物质的溶解进行分析解答即可.
解答 解:(1)硫酸钙能与氨气、二氧化碳和水反应生成碳酸钙沉淀和硫酸铵,故填:CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH4)2SO4;
(2)反应生成的碳酸钙可以循环利用,二氧化碳气体能循环利用,故填:CaCO3、CO2;
(3)硫酸铵能与氯化钾反应生成氯化铵和硫酸钾,是因为在该条件下硫酸钾的溶解度小,故填:(NH4)2SO4+2KCl=2NH4Cl+K2SO4↓;硫酸钾的溶解度最小;
(4)用饱和K2SO4溶液洗涤反应Ⅲ所得K2SO4晶体还可以减少用水洗涤时K2SO4晶体因溶解而造成的损失,故填:减少用水洗涤时K2SO4晶体因溶解而造成的损失.
点评 本题考查的是常见的物质的分离以及提纯的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
20.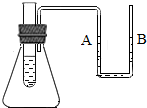 如图,向小试管中分别加入下列一定量的物质,右侧U型管中的液面未发生明显变化.该物质应是( )
如图,向小试管中分别加入下列一定量的物质,右侧U型管中的液面未发生明显变化.该物质应是( )
 如图,向小试管中分别加入下列一定量的物质,右侧U型管中的液面未发生明显变化.该物质应是( )
如图,向小试管中分别加入下列一定量的物质,右侧U型管中的液面未发生明显变化.该物质应是( )| A. | 浓硫酸 | B. | 蔗糖固体 | C. | 氢氧化钠固体 | D. | 氧化钙固体 |
1.下列俗语或成语所涉及的内容只涉及到物理变化的是( )
| A. | 铁杵成针 | B. | 蜡炬成灰 | C. | 烈火真金 | D. | 百炼成钢 |
5.C3N4是一种新型材料,它的硬度比金刚石还高,可做切割工具.在C3N4中,C的化合价为+4,则N的化合价是( )
| A. | -3 | B. | +3 | C. | +1 | D. | +5 |
15.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表所示:下列推理中正确的是( )
| X | Y | Z | Q | |
| 反应前的质量/g | 20 | 80 | 2 | 21 |
| 反应后的质量/g | 4 | 待测 | 38 | 65 |
| A. | 反应后物质Y的质量为44g | |
| B. | 反应中物质X与Y发生改变的质量之比为1:4 | |
| C. | 反应中Z可能是催化剂 | |
| D. | 若X和Z的相对分子质量分别是16和18,则他们的化学计量数之比是2:1 |
