题目内容
17.有一包粉末,已知其由BaCO3、Cu(NO3)2、Na2SO4、NaCl、NaOH中的几种组成,现对其做以下实验,各步骤均已经充分反应,请回答问题: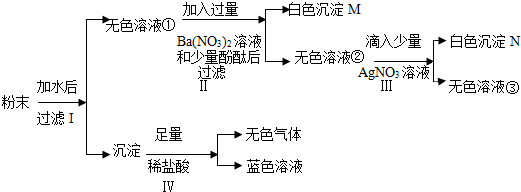
(1)请写出沉淀N的化学式:AgCl.
(2)步骤Ⅱ所发生反应的化学方程式:Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3.
(3)无色溶液②中一定存在的溶质(酚酞除外)的化学式:NaNO3、Ba(NO3)2、NaCl.
分析 根据碳酸钡沉淀难溶于水,硝酸铜和氢氧化钠会生成氢氧化铜沉淀,碳酸钡和盐酸反应会生成二氧化碳,氢氧化铜沉淀和盐酸反应会生成蓝色的氯化铜溶液,硫酸根离子和钡离子会生成硫酸钡沉淀,氯离子和银离子会生成氯化银沉淀等知识进行分析.
解答 (解:碳酸钡沉淀难溶于水,硝酸铜和氢氧化钠会生成氢氧化铜沉淀,碳酸钡和盐酸反应会生成二氧化碳,氢氧化铜沉淀和盐酸反应会生成蓝色的氯化铜溶液,硫酸根离子和钡离子会生成硫酸钡沉淀,氯离子和银离子会生成氯化银沉淀.
粉末加水溶解后,得到沉淀和无色溶液,沉淀中加入盐酸会生成无色气体和蓝色溶液,所以蓝色溶液是氯化铜溶液,沉淀中含有氢氧化铜沉淀,无色粉末中一定含有硝酸铜和氢氧化钠,碳酸钡和盐酸会生成二氧化碳气体,所以粉末中一定含有碳酸钡,无色溶液中加过量的硝酸钡溶液和酚酞,生成白色沉淀M和无色溶液,所以无色溶液中不含氢氧化钠,生成白色沉淀M证明一定含有硫酸钠,无色溶液中加硝酸银会生成白色沉淀N,所以白色沉淀N是氯化银沉淀,粉末中一定含有氯化钠,所以,
(1)通过推导可知,沉淀N是氯化银沉淀,化学式为:AgCl;
(2)步骤Ⅱ所发生的反应是硫酸钠和硝酸钡反应生成硫酸钡沉淀和硝酸钠,化学方程式为:Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3;
(3)无色溶液②和硝酸银会生成氯化银沉淀,所以无色溶液②中含有氯化钠,过量的硝酸钡和硫酸钠反应生成硫酸钡沉淀和硝酸钠,所以溶液②中含有硝酸钡、硝酸钠,所以无色溶液②中一定存在的溶质(酚酞除外)的化学式:NaNO3、Ba(NO3)2、NaCl;
故答案为:
(1)AgCl;(2)Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3;
(3)NaNO3、Ba(NO3)2、NaCl.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

| A. | 矿石粉碎 | B. | 食品发霉 | C. | 湿衣服晾干 | D. | 轮胎爆炸 |
| A. |  巢湖银鱼 | B. |  小岗黑芝麻 | C. |  淮南八公山豆腐 | D. |  怀远石榴 |
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
| 方案 | (1) | (2) | (3) |
| 实验操作 | 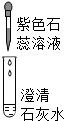 | 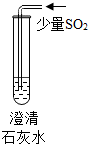 |  |
| 现象 | 溶液变为蓝色 | 澄清石灰水变浑浊 | 红色褪为无色 |
| 结论或解释 | 氢氧化钙溶液能使石蕊等酸碱指示剂变色 | 氢氧化钙溶液能与某些非金属氧化物反应生成盐和水.二氧化硫与澄清石灰水反应的化学方程式是SO2+Ca(OH)2═CaSO3↓+H2O. | 氢氧化钙溶液能与酸发生中和反应 |
【查阅资料】氯化钙溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①氯化钙②氯化钙和氯化氢③氯化钙和氢氧化钙
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙.
探究二:丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴加边振荡.实验后得出产生沉淀质量与碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀,溶液最终变红色.
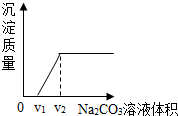
【得出结论】乙同学的猜想中,②(填序号)合理.
【反思讨论】学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化.下列说法正确的是AB(填序号)
A.溶液质量逐渐增大 B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小 D.溶液的pH一直增大.
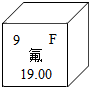 含氟物质的合成,对推动社会进步发挥着巨大作用.
含氟物质的合成,对推动社会进步发挥着巨大作用. ,由氟原子的结构示意图知,氟原子在化学反应中易得(选填“失”或“得”)电子.
,由氟原子的结构示意图知,氟原子在化学反应中易得(选填“失”或“得”)电子.
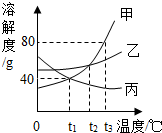 如图是常见固体物质的溶解度曲线,根据图示回答:
如图是常见固体物质的溶解度曲线,根据图示回答: