题目内容
12.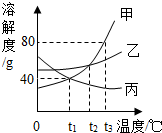 如图是常见固体物质的溶解度曲线,根据图示回答:
如图是常见固体物质的溶解度曲线,根据图示回答:(1)在t2℃时,甲和乙两种物质的溶解度相等.
(2)t1℃时,将140g甲的饱和溶液升温至t3℃时,需要加入40g甲物质,才可能形成饱和溶液.
(3)t3℃时,甲、乙、丙三种物质饱和溶液中溶质的质量分数由大到小的顺序是甲>乙>丙.
(4)t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温至t1℃,没有晶体析出的是丙(填“甲”、“乙”、“丙”).
(5)当甲中含有少量乙时,可以通过降温结晶(或冷却热饱和溶液)的方法提纯甲.
分析 (1)根据交点表示在该温度下二者的溶解度相等解答;
(2)根据该温度下甲的溶解度分析解答;
(3)根据饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%分析解答;
(4)等质量的饱和溶液降低相同的温度,溶解度增大的无晶体析出;
(5)根据固体物质从溶液中结晶析出的方法考虑.
解答 解:(1)在t2℃时,甲和乙两种物质的溶解度曲线交于一点,二者的溶解度相等.
(2)t1℃时甲的溶解度是40g,即100g水中最多溶解40g的甲,所以140g甲的饱和溶液中含有40g的甲,升温至t3℃时,其溶解度变为80g,则需要加入 40g甲物质,才能形成饱和溶液.
(3)t3℃时三种物质的溶解度由大到小的顺序是甲>乙>丙,根据饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%可知溶解度大则溶质的质量分数大,所以甲、乙、丙三种物质饱和溶液中溶质的质量分数由大到小的顺序是甲>乙>丙.
(4)t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温至t1℃,丙的溶解度增大,没有晶体析出.
(5)甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以当甲中含有少量乙时,可以通过降温结晶或冷却热饱和溶液的方法提纯甲;
故答案为:(1)t2;(2)40;(3)甲>乙>丙;(4)丙;(5)降温结晶(或冷却热饱和溶液).
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以知道某温度下物质的溶解度、比较同一温度下不同物质的溶解度大小、提纯物质的方法,并可分析出饱和溶液中溶解度大则溶质的质量分数大等知识,能较好考查学生对知识的掌握和运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列实验的最终现象,不能证明分子总是在不断运动着的是( )
| A. | 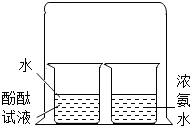 | B. | 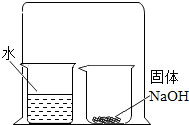 | ||
| C. | 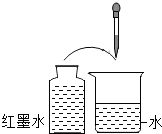 | D. | 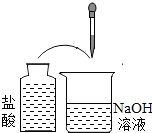 |
20.下列实验方法不正确的是( )
| A. | 用BaCl2溶液鉴别Na2SO4溶液和AgNO3溶液 | |
| B. | 用澄清石灰水鉴别氮气和二氧化碳 | |
| C. | 用闻气味的方法鉴别白酒和白醋 | |
| D. | 用肥皂水鉴别硬水和软水 |
4.根据生活经验和所学知识判断,下列生活中的活动不正确的是( )
| A. | 用点燃的蜡烛伸入山洞检验洞中二氧化碳的浓度高低 | |
| B. | 用将熟石灰与硫酸铵化肥混合施放在田里,提高肥效 | |
| C. | 用热的纯碱溶液清洗餐具上的油污 | |
| D. | 用聚乙烯保鲜膜塑料密封包裹吃剩下的饭菜,防止变质 |