题目内容
11.实验小组同学想得到较纯净的二氧化碳用于后续实验,选用的装置、试剂和操作如下图所示.
(1)A中反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)B装置的作用是干燥二氧化碳.
(3)利用此装置得到的二氧化碳中会含有较多的杂质是氯化氢,因此需要进行实验改进.
(4)C、D为两种验满二氧化碳的方法,其中正确的是C(填字母序号).
分析 (1)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的化学方程式;
(2)根据浓硫酸有吸水性分析;
(3)考虑浓盐酸的挥发性;
(4)考虑二氧化碳的验满方法.
解答 解:(1)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)浓硫酸具有吸水性,可以干燥二氧化碳;
(3)因为盐酸有挥发性,故产生的二氧化碳中混有氯化氢杂质,因此需要进行实验改进;
(4)把燃烧的木条放在集气瓶瓶口,若木条立即熄灭,说明装满,故选C.
故答案为:
(1)CaCO3+2HCl═CaCl2+CO2↑+H2O;(2)干燥二氧化碳;(3)氯化氢;(4)C.
点评 本题考查了二氧化碳的制取及性质的检验,关键要明确二氧化碳本身不显酸性,是二氧化碳和水反应的结果,然后逐一分析即可.

练习册系列答案
相关题目
1.现有一定量的硫酸铜和硫酸的混合溶液,为测定其中硫酸铜的质量,将其让如烧杯中,然后用一溶质质量分数的氢氧化钠溶液120g平均分六次加入其中,充分振荡后,实验所得数据见下表,请你分析并进行有关计算:
(1)上表中X的数值为4.90g;
(2)原混合溶液中硫酸铜的质量;
(3)所用氢氧化钠溶液的质量分数.
| 1 | 2 | 3 | 4 | 5 | 6 | |
| 加入氢氧化钠溶液的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
| 生成沉淀的质量/g | 0 | 2.45 | X | 7.35 | 9.8 | 9.8 |
(2)原混合溶液中硫酸铜的质量;
(3)所用氢氧化钠溶液的质量分数.
19.除去下列各物质中混有的少量杂质,所用试剂、方法正确的是( )
| 序号 | 物质 | 杂质 | 试剂、方法 |
| A | ZnSO4溶液 | CuSO4 | 过量锌粉,过滤 |
| B | Fe粉 | Cu粉 | 稀盐酸,过滤 |
| C | MgCl2溶液 | 盐酸 | 适量的氢氧化钠溶液 |
| D | CO2 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
16.下列空气成分中,常用于充入食品包装袋起防腐作用的是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
3.工业用盐中含有的亚硝酸钠(NaNO2)是一种有毒物质,利用 NH4Cl溶液可使NaNO2转化为无毒物质.该反应分两步进行:①NaNO2+NH4Cl═NaCl+NH4NO2②NH4NO2═N2↑+2H2O
下列叙述不正确的是( )
下列叙述不正确的是( )
| A. | NH4NO2由三种元素组成 | |
| B. | 反应①为复分解反应,反应②为分解反应 | |
| C. | 利用 NH4Cl 处理NaNO2最终转化为NaCl、N2和H2O | |
| D. | 上述反应所涉及的物质中,氮元素的化合价有四种 |
1.下列有关物质的性质、用途等说法正确的是( )
①干冰用于人工降雨
②石墨可作电极
③氧气可用作燃料
④氮气可以用作保护气体
⑤活性炭作口罩滤芯
⑥生活中可用氢氧化钠来除去炉具上的油污,也可治疗胃酸过多.
①干冰用于人工降雨
②石墨可作电极
③氧气可用作燃料
④氮气可以用作保护气体
⑤活性炭作口罩滤芯
⑥生活中可用氢氧化钠来除去炉具上的油污,也可治疗胃酸过多.
| A. | ①②③④⑤⑥ | B. | ①②③④ | C. | ①②④⑤ | D. | ①③④⑥ |
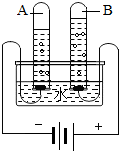 如图是电解水的实验简图,若A试管中产生10mL气体,则B试管中产生5mL气体.
如图是电解水的实验简图,若A试管中产生10mL气体,则B试管中产生5mL气体. 2015年1月起,国内重型柴油机普推国\*MERGEFORMAT IV排放标准.减排的原理为:向反应罐内喷入车用尿素[CO(NH2)2]溶液.在一定条件下,尿素先转化为NH3,NH3再与发动机排出的NO等反应生成氮气和水.
2015年1月起,国内重型柴油机普推国\*MERGEFORMAT IV排放标准.减排的原理为:向反应罐内喷入车用尿素[CO(NH2)2]溶液.在一定条件下,尿素先转化为NH3,NH3再与发动机排出的NO等反应生成氮气和水.