��Ŀ����
8��ͼΪʵ������ȡ����ij���װ�ã������ʵ��װ�ûش����⣮
��1��ͼ�б��������������a�ƾ��ƣ�bˮ�ۣ�
��2����A��C��ϣ���������ʵ������ȡ���ռ���������O2����Ӧ�Ļ�ѧ����ʽΪ2KClO3$\frac{\underline{MnO_2}}{��}$2KCl+3O2����
��3��ʵ�����ø��������ȡ��������Ҫʵ�鲽���У��ټ��ȣ������Թ���װҩƷ���ۼ��װ�������ԣ�������ˮ���ռ���������ֹͣ���ȣ������ܴ�ˮ����ȡ������ȷ��ʵ�����˳���Ǣۢڢ٢ܢޢݣ�����ţ���
��4��BҲ����Ϊ��ȡ�����ķ���װ�ã���A��ȣ�B���ŵ��в��ü��ȣ�������㣨ֻдһ��������Ӧ�Ļ�ѧ����ʽΪ2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2��
��5���о���˿�ڴ�����ȼ��ʱ������ƿ��ˮ�������Ƿ�ֹ���ɵĸ��������ヲ��ƿ�ף�ʹ����ƿը�ѣ�
��6����֪���ռ�������̼ͨ����Dװ�ã�����ѡ��C��Eװ�ã����ܵ�ԭ���ǣ�������̼������ܶȱȿ���������ˮ��
��7��ʵ���ҳ��ü��ȴ����ƺͼ�ʯ�ҵĹ�����������ȡ���飨CH4�����壬������һ����ɫ��ζ���ܶȱȿ���С����������ˮ�����壮�Ƽ���ʱ������ķ���װ����A��������ռ�װ�ÿ�ѡ��C��E��
���� ��ȡװ�ð������ȺͲ���������֣������˫��ˮ�������Ͳ���Ҫ���ȣ�����ø�����ػ����������������Ҫ���ȣ��������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ���ʵ�������������ȡ��������Ҫʵ�鲽���У����װ�������ԣ����Թ���װҩƷ�����ȣ�����ˮ���ռ������������ܴ�ˮ����ȡ����ֹͣ���ȣ����װ�������Եķ����ǣ����Ӻ�װ�ã������ܿڽ�û��ˮ����Һ���£����ֽ����Թܣ������ܿ�������ð������װ�����������ã�BҲ����Ϊ��ȡ�����ķ���װ�ã���A��ȣ�B���ŵ��У����ü��ȣ�������㣻���ڿ��Ʒ�Ӧ���ʵȣ�ʵ������ȡCO2�����ڳ����£���̼��ƺ����ụ�ཻ���ɷ������Ȼ��ƺ�ˮ�Ͷ�����̼����˲���Ҫ���ȣ�������̼������ˮ���ܶȱȿ������ܶȴ����ֻ���������ſ������ռ�����˿�ڴ�����ȼ��ʱ������ƿ��ˮ�������ǣ���ֹ���ɵĸ��������ヲ��ƿ�ף�ʹ����ƿը�ѣ�
��� �⣺��1��ͼ�б�������������Ǿƾ��ơ�ˮ�ۣ��ʴ�Ϊ���ƾ��ơ�ˮ�ۣ�
��2����A��C��ϣ���������ʵ������ȡ���ռ���������O2����Ϊ�Թ�����������������ڶ������̵Ĵ������¼��������Ȼ��غ���������Ӧ�Ļ�ѧ����ʽΪ��2KClO3$\frac{\underline{MnO_2}}{��}$2KCl+3O2����
��3��ʵ�����ø��������ȡ��������Ҫʵ�鲽���У����װ�������ԣ����Թ���װҩƷ�����ȣ�����ˮ���ռ������������ܴ�ˮ����ȡ����ֹͣ���ȣ�����ȷ��ʵ�����˳���ǣ��ۢڢ٢ܢޢݣ�
��4��BҲ����Ϊ��ȡ�����ķ���װ�ã���A��ȣ�B���ŵ��У����ü��ȣ�������㣻���ڿ��Ʒ�Ӧ���ʵȣ����������ڶ������̵Ĵ�����������ˮ����������Ӧ�Ļ�ѧ����ʽΪ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
�ʴ�Ϊ�����ü��ȣ�������㣻���ڿ��Ʒ�Ӧ���ʣ���ѡһ����ֻҪ����������Ҳ�ɣ���2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
��5����˿�ڴ�����ȼ��ʱ������ƿ��ˮ�������ǣ���ֹ���ɵĸ��������ヲ��ƿ�ף�ʹ����ƿը�ѣ��ʴ�Ϊ����ֹ���ɵĸ��������ヲ��ƿ�ף�ʹ����ƿը�ѣ�
��6����֪���ռ�������̼ͨ����Dװ�ã�����ѡ��C��Eװ�ã����ܵ�ԭ���ǣ�������̼������ܶȱȿ���������ˮ��
��7��ʵ���ҳ��ü��ȴ����ƺͼ�ʯ�ҵĹ�����������ȡ�������壬�����Ҫ���ȣ�������һ����ɫ��ζ���ܶȱȿ���С����������ˮ�����壬��˼�������������ſ���������ˮ���ռ����ʴ�Ϊ��A��C��E��
�ʴ�Ϊ��
��1���ƾ��ƣ�ˮ�ۣ���2��O2��2KClO3$\frac{\underline{MnO_2}}{��}$2KCl+3O2������3���ۢڢ٢ܢޢݣ�
��4�����ü��ȣ�������㣬2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2������5����ֹ���ɵĸ��������ヲ��ƿ�ף�ʹ����ƿը�ѣ�
��6��������̼������ܶȱȿ���������ˮ����7��A��C��E��
���� ��������Ҫ�������������ơ��������ȡװ�ú��ռ�װ�õ�ѡ��ͬʱҲ�����˻�ѧ����ʽ����д���ۺ��ԱȽ�ǿ���������ȡװ�õ�ѡ���뷴Ӧ���״̬�ͷ�Ӧ�������йأ�������ռ�װ�õ�ѡ����������ܶȺ��ܽ����йأ����������п�����Ҫ����֮һ����Ҫ������ʵ�����У�

| A�� | �����ijɷְ������������㣬����Լռ78%������Լռ21% | |
| B�� | ϡ�����嶼û����ɫ��û����ζ����ѧ���ʺܲ����� | |
| C�� | ������һ��ʮ����Ҫ����Դ | |
| D�� | ��ҵ�Ϸ���Һ̬������������û������ѧ�仯 |
| �� | �� | �� | �� | |
| ��Ӧǰ��������/% | 70 | 15 | 6.25 | 8.75 |
| ��Ӧ����������/% | 35 | 7.5 | 48.75 | 8.75 |
| A�� | ��һ���������Ӧ�Ĵ��� | |
| B�� | �÷�Ӧ�����ǷֽⷴӦ | |
| C�� | ��һ���ǻ������һ���ǵ��� | |
| D�� | �μӷ�Ӧ�ļ��ҵ�����֮��һ���������ɵı������� |
| A�� | һ����̼��Co | B�� | ������ԭ�ӣ�O2 | ||
| C�� | �������������ӣ�2OH- | D�� | ����þ��þԪ�صĻ��ϼۣ�$\stackrel{+2}{Mg}$O |
| A�� | ʹ�ý�ˮ��ͷ | B�� | ����ࡢ�ι�ķ������ֻ�ũ�� | ||
| C�� | ����ҵ��ˮ���������ŷ� | D�� | ˢ����ϴ��ʱ����Ϸ�ˮ |
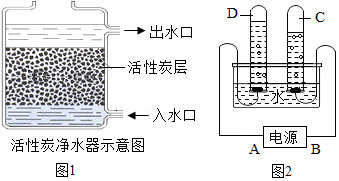 ˮ��������ԴȪ��Ҳ�Dz���ȱ�ٵ���Դ��
ˮ��������ԴȪ��Ҳ�Dz���ȱ�ٵ���Դ�� ijͬѧ�����ǵĺ�ˮ��Ʒ�����ձ����ȼ���������ĩ�����ܽ⣬����һ���������ͼ��ʾ��װ�ý��й��ˣ���ش�
ijͬѧ�����ǵĺ�ˮ��Ʒ�����ձ����ȼ���������ĩ�����ܽ⣬����һ���������ͼ��ʾ��װ�ý��й��ˣ���ش�  ���͡�
���͡� ���ֱ��ʾ���ֲ�ͬԪ�ص�ԭ�ӣ���ô���б�ʾ�������ǣ�������
���ֱ��ʾ���ֲ�ͬԪ�ص�ԭ�ӣ���ô���б�ʾ�������ǣ�������


