题目内容
18.下列实验操作中,正确的是( )| A. |  给试管内液体加热 | B. |  向试管中滴加液体 | ||
| C. |  过滤液体 | D. |  向试管中倾倒液体 |
分析 A、根据给试管内液体加热的注意事项考虑;
B、根据滴管的用法考虑;
C、根据过滤的操作方法考虑;
D、根据液体药品的取用方法考虑.
解答 解:A、给试管中的液体加热时,液体不超过试管容积的三分之一,以防加时沸腾溅出伤人,故A错误;
B、用滴管滴加液体时,需将滴管竖直悬空滴加,不能伸入试管内,故B错误;
C、过滤时:要“一贴”、“二低”、“三靠”;图示操作无玻璃棒引流,故C错误;
D、打开试剂瓶后,瓶塞要倒放,瓶塞正放可能会腐蚀桌面,再放回试剂瓶上时会污染试剂;倒液体时,标签要向着手心,防止倾倒液体时的残留液流出时,腐蚀标签而看不清试剂的名称了.倾倒时要瓶口和试管口紧靠,故D正确.
故选D.
点评 要熟记常见仪器的名称、性质和用法,不要在做实验时进行错误操作.否则会带来一些不安全因素.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.将60g镁、铁、铝的混合物放入到一定质量的稀硫酸中恰好完全反应,收集到氢气4g,将反应后的溶液蒸干可得硫酸盐的质量是( )
| A. | 202g | B. | 256g | C. | 252g | D. | 不能确定 |
2.如图是初中化学常见的一些物质之间的转化.其中说法不正确的是( )


| A. | 反应①中CO发生氧化反应 | |
| B. | 反应②的化学方程式是:Fe+Cu(OH)2=Cu+Fe(OH)2 | |
| C. | X溶液可能是硫酸铜溶液 | |
| D. | 反应③可以检验二氧化碳气体 |
13.下图所示实验操作正确的是( )
| A. |  滴加液体 | B. |  稀释浓硫酸 | C. |  熄灭酒精灯 | D. |  称量氢氧化钠 |
10.我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验.
资料摘要:Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
【方案一】样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
(2)分析滴加的CaCl2溶液要过量的原因:与碳酸钠充分反应.
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算出Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大.
【方案二】样品与稀硫酸反应,测定Na2CO3的质量分数
利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀硫酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好且每步反应或作用都是完全的).

(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,再接上装置C和D.其目的是防止空气中的二氧化碳对实验结果产生影响.
(5)关闭止水夹K,加入足量的稀硫酸(杂质不与稀硫酸反应),装置A中样品产生气体的化学方程式为Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.该方案中不能用稀盐酸代替稀硫酸的原因是盐酸具有挥发性.
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一段时间的目的是使生成的二氧化碳全部被C装置中的氢氧化钠吸收.根据质量守恒定律,装置C(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).
资料摘要:Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
【方案一】样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算出Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大.
【方案二】样品与稀硫酸反应,测定Na2CO3的质量分数
利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀硫酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好且每步反应或作用都是完全的).

(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,再接上装置C和D.其目的是防止空气中的二氧化碳对实验结果产生影响.
(5)关闭止水夹K,加入足量的稀硫酸(杂质不与稀硫酸反应),装置A中样品产生气体的化学方程式为Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.该方案中不能用稀盐酸代替稀硫酸的原因是盐酸具有挥发性.
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一段时间的目的是使生成的二氧化碳全部被C装置中的氢氧化钠吸收.根据质量守恒定律,装置C(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).
 请用化学用语填空:
请用化学用语填空:

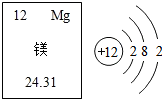 打造更完美的电动汽车,镁电池或将取代锂电池成新一代霸主.(1)元素的相对原子质量为24.31;
打造更完美的电动汽车,镁电池或将取代锂电池成新一代霸主.(1)元素的相对原子质量为24.31;