题目内容
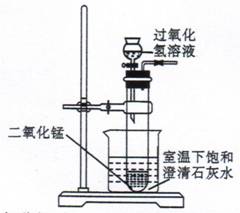
右图是同学们根据所学知识设计的一个趣味实验,请你参与并回答下列问题:
(1)将分液漏斗里的过氧化氢溶液滴人盛有二氧化锰的大试管中。观察到试管中有
气泡产生,请写出反应的化学方程式 ,该反应的
类型是 。检验生成气体的实验方法 。
反应后发现二氧化锰质量和化学性质未改变,它是反应的 。
(2)过一会看到烧杯中的饱和澄清石灰水变浑浊,说明过氧化氢分解时 (填“吸收”或“放出” )热量;也说明氢氧化钙的溶解度随温度 (填“升高”或“下降” )而减小。
 |
(7分)化学方程式2分,其余每空1分。
(1)2H2O2 MnO2 2H2O+ O2 ↑(2分);分解反应;带火星木条放在导管口,木条复燃;催化剂;
(2)放出;升高。

 53随堂测系列答案
53随堂测系列答案下列数据是硝酸钾固体在不同温度时的溶解度。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(1)由上表可得到的信息是 。
(2)20℃时,向100 g水中加入31.6 g硝酸钾,充分溶解后得到 (填“饱和”或“不饱和”)溶液。
(3)20℃时,向100 g水中加入40 g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是 。
(4)某标签上 标有“16%的硝酸钾溶液”,由该标签可获得的信息是 、 。
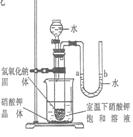
(5)右图是同学们根据所学知识设计的一个趣味实验,请参与实验 并回答问题:将分液漏斗里适量的水加入大试管中,使足够量的氢氧 化钠固体完全溶解后,能观察到的现象是 ;
请解释产生上述现象的主要原因是
。
 8、右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:
8、右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题: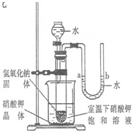 下列数据是硝酸钾固体在不同温度时的溶解度.
下列数据是硝酸钾固体在不同温度时的溶解度.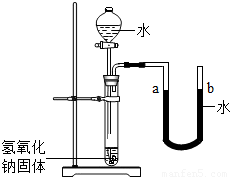 右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:
右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题: