题目内容
 8、右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:
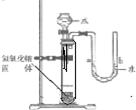
8、右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:将分液漏斗里适量的水加人大试管中,使足够量的氢氧化钠固体完全溶解后,能观察到的现是
U型管中,a端水位下降,b端水位上升
;产生上述现象的主要原因是
氢氧化钠固体溶于水,放热,使试管内的气压升高.
.分析:氢氧化钠虽然不能与水发生反应,但是氢氧化钠溶解时却会放出大量的热,使装置内气体受热膨胀气体体积变大,U型管内液体会向外流动.
解答:解:氢氧化钠溶于水放出大量的热,装置内气体受热膨胀体积变大压强变大,U型管内左侧液面(a端)下降,右侧液面(b端)上升.
故答:U型管中,a端水位下降,b端水位上升;氢氧化钠固体溶于水,放热,使试管内的气压升高.
故答:U型管中,a端水位下降,b端水位上升;氢氧化钠固体溶于水,放热,使试管内的气压升高.
点评:氢氧化钠易溶于水,置于空气中的氢氧化钠固体会吸收空气中的水而潮解,氢氧化钠常用作干燥剂.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
下列数据是硝酸钾固体在不同温度时的溶解度。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(1)由上表可得到的信息是 。
(2)20℃时,向100 g水中加入31.6 g硝酸钾,充分溶解后得到 (填“饱和”或“不饱和”)溶液。
(3)20℃时,向100 g水中加入40 g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是 。
(4)某标签上 标有“16%的硝酸钾溶液”,由该标签可获得的信息是 、 。
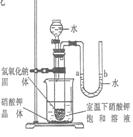
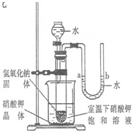
(5)右图是同学们根据所学知识设计的一个趣味实验,请参与实验 并回答问题:将分液漏斗里适量的水加入大试管中,使足够量的氢氧 化钠固体完全溶解后,能观察到的现象是 ;
请解释产生上述现象的主要原因是
。
 下列数据是硝酸钾固体在不同温度时的溶解度.
下列数据是硝酸钾固体在不同温度时的溶解度.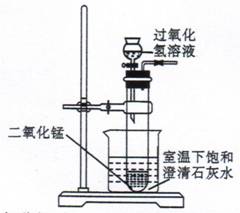
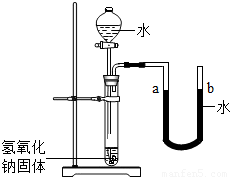 右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:
右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题: