题目内容
 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加一定质量分数的Na2SO4溶液.下图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算:
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加一定质量分数的Na2SO4溶液.下图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算:(1)生成沉淀的质量是______g.
(2)所加 Na2SO4溶液的溶质质量分数?
(3)求恰好完全反应时,所得溶液中溶质的质量分数为多少?
【答案】分析:向氯化钠和氯化钡的混合溶液中加入硫酸钠溶液,氯化钡会与硫酸钠反应生成硫酸钡沉淀和氯化钠.
(1)从图中可明显看出沉淀的质量.
(2)写出氯化钡与硫酸钠反应的化学方程式,根据沉淀的质量求出参加反应的硫酸钠的质量,再从图中找出恰好完全反应时所加的硫酸钠溶液的质量,最后根据 ×100%求出硫酸钠溶液中溶质的质量分数.
×100%求出硫酸钠溶液中溶质的质量分数.
(3)所得溶液中溶质的质量分数= ×100%,溶质是氯化钠,包括原混合物中的氯化钠(根据沉淀的质量求出氯化钡的质量,再用混合物的质量-氯化钡质量)和反应生成的氯化钠(根据沉淀的质量可求出),所得溶液的质量=所加的所有物质的总质量-生成沉淀的质量.
×100%,溶质是氯化钠,包括原混合物中的氯化钠(根据沉淀的质量求出氯化钡的质量,再用混合物的质量-氯化钡质量)和反应生成的氯化钠(根据沉淀的质量可求出),所得溶液的质量=所加的所有物质的总质量-生成沉淀的质量.
解答:解:(1)从图中可看出生成沉淀的质量为23.3g.故答案为:23.3
(2)设参加反应的硫酸钠的质量为x,参加反应的氯化钡的质量为y,生成的氯化钠的质量为z.
BaCl2+Na2SO4=2NaCl+BaSO4↓
208 142 117 233
y x z 23.3g



x=14.2g y=20.8g z=11.7g
 ×100%=14.2% 答:所加硫酸钠溶液中溶质的质量分数为14.2%.
×100%=14.2% 答:所加硫酸钠溶液中溶质的质量分数为14.2%.
(3)所得溶液中溶质的质量分数= ×100%=10%
×100%=10%
答:所得溶液中溶质的质量分数是10%.
点评:求反应后所得溶液的质量的方法一般是用所加的所有物质的质量总和-生成气体的质量-生成沉淀的质量.
(1)从图中可明显看出沉淀的质量.
(2)写出氯化钡与硫酸钠反应的化学方程式,根据沉淀的质量求出参加反应的硫酸钠的质量,再从图中找出恰好完全反应时所加的硫酸钠溶液的质量,最后根据
 ×100%求出硫酸钠溶液中溶质的质量分数.
×100%求出硫酸钠溶液中溶质的质量分数.(3)所得溶液中溶质的质量分数=
 ×100%,溶质是氯化钠,包括原混合物中的氯化钠(根据沉淀的质量求出氯化钡的质量,再用混合物的质量-氯化钡质量)和反应生成的氯化钠(根据沉淀的质量可求出),所得溶液的质量=所加的所有物质的总质量-生成沉淀的质量.
×100%,溶质是氯化钠,包括原混合物中的氯化钠(根据沉淀的质量求出氯化钡的质量,再用混合物的质量-氯化钡质量)和反应生成的氯化钠(根据沉淀的质量可求出),所得溶液的质量=所加的所有物质的总质量-生成沉淀的质量.解答:解:(1)从图中可看出生成沉淀的质量为23.3g.故答案为:23.3
(2)设参加反应的硫酸钠的质量为x,参加反应的氯化钡的质量为y,生成的氯化钠的质量为z.
BaCl2+Na2SO4=2NaCl+BaSO4↓
208 142 117 233
y x z 23.3g



x=14.2g y=20.8g z=11.7g
 ×100%=14.2% 答:所加硫酸钠溶液中溶质的质量分数为14.2%.
×100%=14.2% 答:所加硫酸钠溶液中溶质的质量分数为14.2%.(3)所得溶液中溶质的质量分数=
 ×100%=10%
×100%=10%答:所得溶液中溶质的质量分数是10%.
点评:求反应后所得溶液的质量的方法一般是用所加的所有物质的质量总和-生成气体的质量-生成沉淀的质量.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
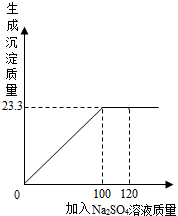 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(ρ水=1lg/cm3),向所得溶液中滴加质量分数为14.2%的Na2SO4溶液,至恰好完全反应,下图是所加Na2SO4溶液质量与生成沉淀质量的关系图.
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(ρ水=1lg/cm3),向所得溶液中滴加质量分数为14.2%的Na2SO4溶液,至恰好完全反应,下图是所加Na2SO4溶液质量与生成沉淀质量的关系图.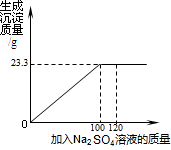 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加质
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加质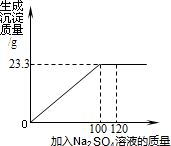 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加一定质量分数的Na2SO4溶液.下图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算:
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加一定质量分数的Na2SO4溶液.下图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算: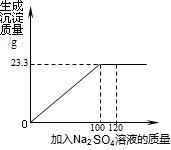 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加质
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加质