题目内容
 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加质
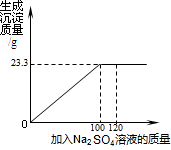
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加质量分数为14.2% 的Na2SO4溶液.右下图是所加Na2SO4溶液质量与生成沉淀质量的关系图,
计算(1)生成23.3g沉淀时,滴加的Na2SO4溶液中含Na2SO4的质量是
(2)恰好完全反应时所得溶液的溶质质量分数.
分析:(1)根据正确书写的化学反应方程式,计算生成23.3g沉淀时,滴加的Na2SO4溶液中含Na2SO4的质量;
(2)根据溶液中溶质的质量分数=
×100%,溶质是氯化钠,包括原混合物中的氯化钠(根据沉淀的质量求出氯化钡的质量,再用混合物的质量-氯化钡质量)和反应生成的氯化钠(根据沉淀的质量可求出),所得溶液的质量=所加的所有物质的总质量-生成沉淀的质量,进行解答.
(2)根据溶液中溶质的质量分数=
| 溶质的质量 |
| 溶液的质量 |
解答:解:(1)生成23.3g沉淀时,滴加的Na2SO4溶液中含Na2SO4的质量为 M
BaCl2 +Na2SO4 =BaSO4↓+2NaCl
142 233
M 23.3g
=
M=14.2 g; 故答案为:14.2g;
(2)设原混合物中含有BaCl2的质量为x,反应生成NaCl的质量为y
BaCl2+Na2SO4=BaSO4↓+2NaCl
208 233 117
x 23.3g y
=
,x=20.8g;
=
,y=11.7g;
溶质氯化钠的质量:(29.1g-20.8g)+11.7g=20g
溶液的质量:29.1g+94.2g+100g-23.3g=200g
溶液中溶质的质量分数=
×100%=10%;
答:恰好完全反应时所得溶液的溶质质量分数为10%.
BaCl2 +Na2SO4 =BaSO4↓+2NaCl
142 233
M 23.3g
| 142 |
| 233 |
| M |
| 23.3g |
(2)设原混合物中含有BaCl2的质量为x,反应生成NaCl的质量为y
BaCl2+Na2SO4=BaSO4↓+2NaCl
208 233 117
x 23.3g y
| 208 |
| x |
| 233 |
| 23.3g |
| 117 |
| y |
| 233 |
| 23.3g |
溶质氯化钠的质量:(29.1g-20.8g)+11.7g=20g
溶液的质量:29.1g+94.2g+100g-23.3g=200g
溶液中溶质的质量分数=
| 20 |
| 200 |
答:恰好完全反应时所得溶液的溶质质量分数为10%.
点评:求反应后所得溶液的质量的方法一般是:用所加的所有物质的质量总和-(减去)生成气体的质量-生成沉淀的质量.

练习册系列答案
相关题目
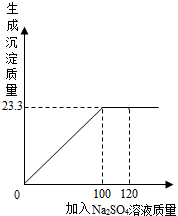 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(ρ水=1lg/cm3),向所得溶液中滴加质量分数为14.2%的Na2SO4溶液,至恰好完全反应,下图是所加Na2SO4溶液质量与生成沉淀质量的关系图.
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(ρ水=1lg/cm3),向所得溶液中滴加质量分数为14.2%的Na2SO4溶液,至恰好完全反应,下图是所加Na2SO4溶液质量与生成沉淀质量的关系图.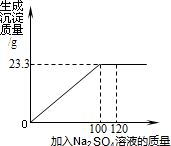 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加一定质量分数的Na2SO4溶液.下图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算:
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加一定质量分数的Na2SO4溶液.下图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算: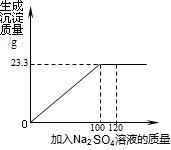 将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加质
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2g水中,向所得溶液中滴加质