题目内容
为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质.其原理是把蛋白质中的氮元素完全转化成氨气
(化学式: ),再用稀硫酸吸收氨气,反应的化学方程式为:
),再用稀硫酸吸收氨气,反应的化学方程式为: .现取该牛奶样品30mL用“盖尔达法”分解其中的蛋白质,产生的氨气用9.5g溶质质量分数为4.9%的稀硫酸恰好完全吸收.计算回答下列问题:
.现取该牛奶样品30mL用“盖尔达法”分解其中的蛋白质,产生的氨气用9.5g溶质质量分数为4.9%的稀硫酸恰好完全吸收.计算回答下列问题:
(1)
产生氨气的质量是多少克?(计算结果精确到0.01,下同)(2)30mL
牛奶中含氮元素的质量是多少克?(3)
下图是该牛奶包装标签的部分内容.已知牛奶中的蛋白质含氮元素的质量分数为16%,请你通过计算确定,该牛奶样品中蛋白质的含量是否达到了包装标签所标示的蛋白质的质量标准.
答案:略
解析:
提示:
解析:
|
(1) 设产生氨气的质量为x.
(2)30mL 牛奶中含氮元素的质量为: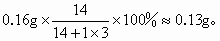
(3)250mL 牛奶中氮元素质量为: 250mL牛奶中蛋白质质量为: 250mL牛奶中蛋白质质量为: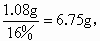 故已达到标准. 故已达到标准.
答:略. 本题主要涉及了两类计算:一类是根据化学方程式的计算.另一类是根据化学式的计算.此题的难点是第 (3)小题,注意学会利用氮元素质量转化为蛋白质质量,从而准确地判断牛奶的质量是否达标. |
提示:
|
用所学的化学知识分析解决生活中实际问题,体现了知识的应用性原则. |

练习册系列答案
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
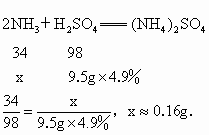
 为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质.其原理是把蛋白质中的氮元素完全转化成氨气(化学式为:NH3),再用稀硫酸吸收氨气,反应的化学方程式:
为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质.其原理是把蛋白质中的氮元素完全转化成氨气(化学式为:NH3),再用稀硫酸吸收氨气,反应的化学方程式: 硫酸铵
硫酸铵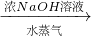 氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问
氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问