题目内容
4.下列(如图1)为实验室常用的实验装置,请回答问题:
(1)写出带有标号仪器的名称:a酒精灯;b水槽.
(2)用高锰酸钾制取氧气的反应方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,用排水法收集氧气的合适时机是气泡连续均匀冒出时,开始收集.
(3)实验室用稀硫酸和锌反应制取干燥的H2,应选用的装置组合是AC,反应的化学方程式是Zn+H2SO4=ZnSO4+H2↑.
(4)装置A虽然操作简便,但无法控制反应速率.请从图2中选取Ⅲ(填序号)取代A中的单孔塞,以达到控制反应速率的目的.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,以及实验室制取氧气的注意事项进行分析;
(3)根据实验室制取氢气的反应物是固体和液体,反应条件是常温,排水法收集的气体纯净,排空气法收集的气体干燥,氢气密度比空气小,锌和硫酸反应生成硫酸锌和氢气进行分析;
(4)根据注射器可以控制液体的滴加速度进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是酒精灯,b是水槽;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,用排水法收集氧气的合适时机是:气泡连续均匀冒出时,开始收集;
(3)实验室制取氢气的反应物是固体和液体,反应条件是常温,排水法收集的气体纯净,排空气法收集的气体干燥,氢气密度比空气小,所以应选用的装置组合是AC,锌和硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(4)注射器可以控制液体的滴加速度,所以选取Ⅲ取代A中的单孔塞,以达到控制反应速率的目的.
故答案为:(1)酒精灯,水槽;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,气泡连续均匀冒出时,开始收集;
(3)AC,Zn+H2SO4=ZnSO4+H2↑;
(4)Ⅲ.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.火锅店服务员用锅盖熄灭酒精灯火锅,其灭火原理是( )
| A. | 清除可燃物 | B. | 使可燃物与氧气隔绝 | ||
| C. | 降低可燃物的着火点 | D. | 使可燃物的温度降低到着火点以下 |
15.对下列化学用语解释正确的是( )
| A. | Mg+--镁离子 | B. | O2--两个氧原子 | C. | 2H2--两个氢分子 | D. | 2N--两个氮元素 |
12.创建文明卫生城市,保护环境人人有责.下列措施有利于环境保护的是( )
①超市和商城等对塑料袋实行有偿使用
②倡导公共大交通,减少机动车燃油排放含氮、硫的氧化物的量
③在太湖流域的每个城市建设生活污水处理设施
④大量使用农药、化肥,以提高农作物产量
⑤露天焚烧处理生活垃圾和农作物秸秆.
①超市和商城等对塑料袋实行有偿使用
②倡导公共大交通,减少机动车燃油排放含氮、硫的氧化物的量
③在太湖流域的每个城市建设生活污水处理设施
④大量使用农药、化肥,以提高农作物产量
⑤露天焚烧处理生活垃圾和农作物秸秆.
| A. | ①②③ | B. | ②③④ | C. | ①②③④ | D. | ①②③④⑤ |
19.“塑化剂”是一种重要的工业原料,但被不法商人添加到商品中,造成了“塑化剂风波”.已知“塑化剂”的化学式为C12H34O4,下列说法不正确的是( )
| A. | “塑化剂”由46个原子构成 | |
| B. | “塑化剂”由碳、氢、氧三种元素组成 | |
| C. | “塑化剂”中碳氢氧原子个数比为12:34:4 | |
| D. | 商品添加剂要严格按照国家规定标准进行使用 |
9.下列各组物质可以按照指定顺序进行直接转化的是( )
| A. | S→SO2→Na2SO4→NaOH | B. | HCl→NaCl→CaCl2→HCl | ||
| C. | CO2→Na2CO3→CaCO3→CO2 | D. | Fe→Fe2O3→FeSO4→Fe |
16.现有下列物质:①氢气;②明矾;③二氧化碳;④二氧化硫.按要求填空(只填序号):
①最清洁的燃料是①; ②能使澄清石灰水变浑浊的无色无味气体是③;
③常见的一种大气污染物是④;④常用于净水的物质是②.
①最清洁的燃料是①; ②能使澄清石灰水变浑浊的无色无味气体是③;
③常见的一种大气污染物是④;④常用于净水的物质是②.
15.复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个探究实验.
探究1:研究常见物质组成

A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的元素组成来推断水的组成的.而C实验与B(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
探究3:研究常见物质制取--制取氢氧化钠溶液
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”他提出了如下实验:
小妮认为小欢的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是碳酸钠溶液也能使酚酞试液变红色.
小妮设计了另一个实验:
我认为:小欢和小妮的实验是为了证实小京结论的可靠性,小京的结论不可靠,原因
是氢氧化钠溶液中含有碳酸钠.显然小妮的实验可靠性比小欢的实验好,原因是排除了碳酸钠溶液的干扰.
探究1:研究常见物质组成

A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的元素组成来推断水的组成的.而C实验与B(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 碳酸钠溶液 | 产生气泡 | 证明研究结论正确 |
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”他提出了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有氢氧化钠 |
小妮设计了另一个实验:
| 实验步骤 | 实验现象 | 实验结论 |
用试管取无色溶液少许,加入过量的氯化钙溶液,再滴加适量的酚酞试液 | 酚酞试液变红色 | 无色溶液中确实 含有氢氧化钠 |
是氢氧化钠溶液中含有碳酸钠.显然小妮的实验可靠性比小欢的实验好,原因是排除了碳酸钠溶液的干扰.
16.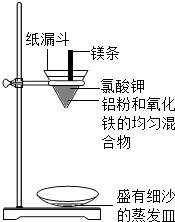 实验二:铝粉和氧化铁粉末反应(铝热反应)
实验二:铝粉和氧化铁粉末反应(铝热反应)
实验装置如图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
【实验总结】金属与金属氧化物在高温条件下有些能反应,有些不能反应.
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.
 实验二:铝粉和氧化铁粉末反应(铝热反应)
实验二:铝粉和氧化铁粉末反应(铝热反应)实验装置如图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成红色 固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈无色. | Mg和CuO能反应 |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.