题目内容
5.下列各组微粒中,属于同一种元素的是( )| A. | H和He | B. | Co和CO | C. | S和S2- | D. |  和 和 |
分析 根据元素是具有相同核电荷数(即核内质子数)的同一类原子的总称,进行分析解答本题.
解答 解:A、H和He的原子内质子数不同,所以是两种不同的元素,故错误;
B、Co是钴的元素符号,CO是一氧化碳,不是一种元素;故错误;
C、S和S2-的核电荷数都是16,不同的是S核外有16个电子,而S2-核外有18个电子,它们具有相同的核电荷数,同属于硫元素;故正确;
D、两种微粒的质子数(核电荷数)不同,不属于同一种元素.故错误.
故选C.
点评 本题考查学生对元素的概念的理解与掌握,并应用才知识进行分析解题的能力.

练习册系列答案
相关题目
16.下列广告语中,你认为符合科学道理的是( )
| A. | “超纯水”、“超纯蒸馏水”绝对卫生,对人体有益 | |
| B. | 本饮料由纯天然物质配制而成,绝对不含化学物质,对人体无害 | |
| C. | 含氟牙膏可以预防龋齿 | |
| D. | 铅笔不是铅、水银不是银、纯碱不是碱 |
20. 固体铵盐A、B的成分可能是(NH4)2SO4、NH4HSO4,或是两者的混合物.甲、乙两个研究性学习小组的同学想要确定A和B的成分,并测定B中氮元素的质量分数.
固体铵盐A、B的成分可能是(NH4)2SO4、NH4HSO4,或是两者的混合物.甲、乙两个研究性学习小组的同学想要确定A和B的成分,并测定B中氮元素的质量分数.
(1)甲实验小组的同学取了数份相同质量的样品A溶于水,然后加入40% NaOH溶液(图中用氢氧化钠质量表示),水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用足量浓硫酸完全吸收,浓硫酸增重的质量如图.分析该图象并回答下列问题:
①写出a b段涉及的化学方程式:(NH4)2SO4+2NaOH$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4 +2NH3↑+2H2O;
②样品A的成分是(NH4)2SO4和NH4HSO4,c点的数值是4.25.
(2)乙实验小组的同学取了数份不同质量的样品B,测定方法与甲组同学大部分相同,不同的是,他们将不同质量的铵盐分别加入到50.00mLNaOH溶液中(含8.12gNaOH ),测定结果如下:
①分析实验数据可知,实验编号为Ⅰ的实验中,氢氧化钠足量,铵盐中的铵根离子完全转化成气体.
②样品B中氮元素的质量分数为17.00%(保留两位小数).
 固体铵盐A、B的成分可能是(NH4)2SO4、NH4HSO4,或是两者的混合物.甲、乙两个研究性学习小组的同学想要确定A和B的成分,并测定B中氮元素的质量分数.
固体铵盐A、B的成分可能是(NH4)2SO4、NH4HSO4,或是两者的混合物.甲、乙两个研究性学习小组的同学想要确定A和B的成分,并测定B中氮元素的质量分数.(1)甲实验小组的同学取了数份相同质量的样品A溶于水,然后加入40% NaOH溶液(图中用氢氧化钠质量表示),水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用足量浓硫酸完全吸收,浓硫酸增重的质量如图.分析该图象并回答下列问题:
①写出a b段涉及的化学方程式:(NH4)2SO4+2NaOH$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4 +2NH3↑+2H2O;
②样品A的成分是(NH4)2SO4和NH4HSO4,c点的数值是4.25.
(2)乙实验小组的同学取了数份不同质量的样品B,测定方法与甲组同学大部分相同,不同的是,他们将不同质量的铵盐分别加入到50.00mLNaOH溶液中(含8.12gNaOH ),测定结果如下:
| 实验编号 | I | II | III | IV |
| 铵盐的质量(g) | 10.00 | 20.00 | 30.00 | 50.00 |
| 浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
②样品B中氮元素的质量分数为17.00%(保留两位小数).
17.t℃时,把某物质的不饱和溶液分成甲、乙两份,甲份的质量占$\frac{3}{5}$,乙份的质量占$\frac{2}{5}$.在甲份中蒸发m克水或在乙份中加入m克溶质都会成为饱和溶液.t℃时该物质的溶解度为( )
| A. | 100克 | B. | 150克 | C. | 75克 | D. | 67克 |
14.物质之间既有相互联系又存在规律,这是我们学好化学应该掌握的一种基本方法.
按规律填空:
①C2H4、C3H6、C4H8、C5H10、C6H12
②NaCl、Cl2、NaClO、KClO3、HClO4.
按规律填空:
①C2H4、C3H6、C4H8、C5H10、C6H12
②NaCl、Cl2、NaClO、KClO3、HClO4.
15.下列有关溶液、溶解度性质的说法中错误的是( )
| A. | 配制溶液时,搅拌溶液可以增大溶质的溶解度 | |
| B. | 溶液加水稀释前后溶质的质量不变 | |
| C. | 盐酸是氯化氢气体的水溶液,根据气体溶解度变化规律,贮存时要阴凉密封 | |
| D. | 汗水浸湿的衣服晾干后出现白色斑迹,是因为水分蒸发后盐分结晶析出 |
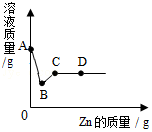 往装有一定质量AgNO3和Cu(NO3)2混合溶液的烧杯中加入Zn,溶液质量与加入Zn的质量关系如图所示.请根据要求回答有关问题.
往装有一定质量AgNO3和Cu(NO3)2混合溶液的烧杯中加入Zn,溶液质量与加入Zn的质量关系如图所示.请根据要求回答有关问题.