题目内容
14.向碳酸钠和氯化钠的混合物15.6g中加入100g稀盐酸,恰好完全反应后,得到111.2g溶液.试计算:(H-1C-12 O-16 Na-23 Cl-35.5)(1)产生二氧化碳4.4克?
(2)所得溶液中溶质质量分数是多少?
分析 根据质量差可以计算生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钠、生成氯化钠的质量,进一步可以计算所得溶液中溶质的质量分数.
解答 解:①产生二氧化碳的质量为:15.6g+100g-111.2g=4.4g,
故填:4.4.
(2)解:设碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
x y 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$,$\frac{117}{y}=\frac{44}{4.4g}$
x=10.6g,y=11.7g,
碳酸钠和氯化钠的混合物中,氯化钠的质量为:15.6g-10.6g=5.0g,
所得溶液中溶质中,溶质氯化钠的质量为:11.7g+5.0g=16.7g,
所得溶液中溶质的质量分数为:$\frac{16.7g}{111.2g}$×100%=15.0%,
答:所得溶液中溶质的质量分数为15.0%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,解答时要注意差量法计算生成二氧化碳质量的简便之处.

练习册系列答案
相关题目
12.将下表的各项内容补充完整:
| 物质 名称 | 碱式碳酸铜 | 二氧化碳 | 水 | 镁 | 氧化镁 | 氧化铜 |
| 颜色 | 绿色 | |||||
| 状态 | 固体 | |||||
| 化学式 | Cu2(OH)2CO3 |
5.下列变化中,属于化学变化的是( )
| A. | 铁铸成锅 | B. | 冰雪融化 | C. | 牛奶变酸 | D. | 苹果榨汁 |
9.“珍爱生命,远离毒品”.冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为C10H15N).有关甲基苯丙胺的说法正确的是( )
| A. | 燃烧只生成二氧化碳和水 | B. | 属于有机物 | ||
| C. | 一个分子中原子总数为25 | D. | 属于混合物 |
4.氢化钙(CaH2)是一种储氢材料,是登山运动员常用的能源提供剂.甲、乙两位同学选用如图装置(固定装置省略),用氢气与金属钙加热制备氢化钙.实验结束后,两位同学对硬质玻璃管中的固体进行如下探究:
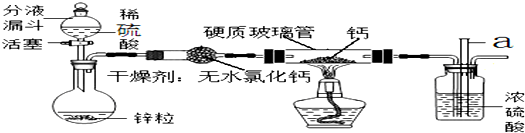
【提出问题】硬质玻璃管中的钙是否完全转化为CaH2?
【查阅资料】
(1)金属钙活动性很强,遇水反应生成氢化钙,同时产生一种气体;
(2)氢化钙要密封保存,遇水反应放出氢气.
【猜想与实验】
(1)固体为Ca和CaH2.
(2)固体为CaH2.
甲同学的探究活动如下:
【实验反思】
乙同学认为由以上探究活动还不能得出猜想1正确,理由是若固体为CaH2,遇水反应也会产生相同的现象,请你帮助乙设计实验,写出主要的实验步骤、现象和相应结论:取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH2;若不相等,则说明Ca未完全转化为CaH2.
【反思讨论】
(1)写出CaH2与水反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是便于携带、避免爆炸危险.
(3)制备CaH2装置中,玻璃管a的作用是检验装置的气密性.

【提出问题】硬质玻璃管中的钙是否完全转化为CaH2?
【查阅资料】
(1)金属钙活动性很强,遇水反应生成氢化钙,同时产生一种气体;
(2)氢化钙要密封保存,遇水反应放出氢气.
【猜想与实验】
(1)固体为Ca和CaH2.
(2)固体为CaH2.
甲同学的探究活动如下:
| 实验操作 | 实验现象 | 实验结论及解释 |
| ①取少量硬质玻璃管中的固体于试管中,滴入少量水,收集产生的气体,并用燃着的木条点燃. | 冒气泡;气体燃烧,产生淡蓝色火焰 | 有氢气生成 |
| ②继续向溶液中滴加酚酞. | 呈红色 | 生成Ca(OH)2(填化学式) |
乙同学认为由以上探究活动还不能得出猜想1正确,理由是若固体为CaH2,遇水反应也会产生相同的现象,请你帮助乙设计实验,写出主要的实验步骤、现象和相应结论:取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH2;若不相等,则说明Ca未完全转化为CaH2.
【反思讨论】
(1)写出CaH2与水反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是便于携带、避免爆炸危险.
(3)制备CaH2装置中,玻璃管a的作用是检验装置的气密性.

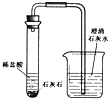 在盛有少量石灰石的试管里加入适量稀盐酸,并将导管的一段伸入装有澄清石灰石的烧杯中,依据实验回答下列问题:
在盛有少量石灰石的试管里加入适量稀盐酸,并将导管的一段伸入装有澄清石灰石的烧杯中,依据实验回答下列问题: