题目内容
5.三氯异氰尿酸(C303N3C13)是一种高效消毒剂,又称高氯精.下列有关高氯精的说法不正确的是( )| A. | 高氯精由4种元素组成 | |
| B. | 高氯精中氯元素的质量分数为25% | |
| C. | 高氯精中C、N两种元素的质量比为6:7 | |
| D. | 高氯精中C、O、N、Cl的原子个数比为1:l:1:1 |
分析 A.根据高氯精的化学式C303N3Cl3 进行分析其元素组成;
B.根据化合物中某元素的质量分数计算方法来分析;
C.根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
D.根据标在元素符号右下角的数字表示一个分子中所含原子的个数;进行解答.
解答 解:A.根据高氯精的化学式C303N3Cl3 可知高氯精由C、O、N、Cl四种元素组成;故正确;
B.高氯精中氯元素的质量分数=$\frac{35.5×3}{77.5×3}×100%$=45.8%;故错误;
C.根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可知高氯精中C、N两种元素的质量比为:12×3:14×3=12:14=6:7; 故正确;
D.根据标在元素符号右下角的数字表示一个分子中所含原子的个数;可知高氯精中C、O、N、Cl的原子个数比为:3:3:3:3=1:1:1:1;故正确;
故选B.
点评 本题考查学生对物质的组成,化合物中各元素质量比,化合物中某元素的质量分数知识的理解与掌握,并能在解题中灵活应用.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
15.实验探究
氢气是一种密度比空气小、难溶于水的气体.实验室常用金属锌和硫酸溶液来制取少量氢气,反应的化学方程为:Zn+H2SO4═ZnSO4+H2↑.化学兴趣小组的同学根据实验室提供的仪器和药品,进行了如下探究实验.
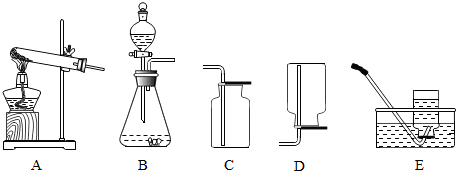
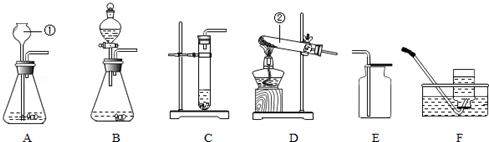
(1)制取氢气可选择图中的(填编号)B,选择此发生装置的理由是氢气的制取是固体和液体在常温下反应,若用此发生装置制取氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)小兵对“锌和硫酸反应快慢的影响因素”进行了探究.
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】
a.可能与硫酸溶液的浓度有关;
b.可能与锌的形状有关;
…
【设计并实验】小兵用不同浓度的硫酸溶液和不同形状的锌进行实验,记录如表所示.
对照实验是实验中只有一个变量,其他的量都保持不变.请你指出小兵实验中的对照实验(填实验编号)和变量(同种变量不重复得分).
第①组对照实验AC,变量硫酸的浓度(或质量分数);
第②组对照实验AB或CD,变量锌粒的形状.
【获得结论】
分析表中数据,可以得出的结论是硫酸的质量分数越大,反应速率越快;锌与硫酸的接触面积越大,反应速率越快;
【实验反思】
锌与硫酸溶液反应的快慢还可能受哪些因素影响?设计实验验证之.温度,取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间(只要有控制变量的意识即可).
氢气是一种密度比空气小、难溶于水的气体.实验室常用金属锌和硫酸溶液来制取少量氢气,反应的化学方程为:Zn+H2SO4═ZnSO4+H2↑.化学兴趣小组的同学根据实验室提供的仪器和药品,进行了如下探究实验.

(1)制取氢气可选择图中的(填编号)B,选择此发生装置的理由是氢气的制取是固体和液体在常温下反应,若用此发生装置制取氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)小兵对“锌和硫酸反应快慢的影响因素”进行了探究.
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】
a.可能与硫酸溶液的浓度有关;
b.可能与锌的形状有关;
…
【设计并实验】小兵用不同浓度的硫酸溶液和不同形状的锌进行实验,记录如表所示.
| 实验编号 | 硫酸溶液的浓度 (均取20mL) | 锌的形状 (均取1g) | 气体的体积(mL) (均收集3分钟) |
| A | 20% | 锌粒 | 31.7 |
| B | 20% | 锌片 | 50.9 |
| C | 30% | 锌粒 | 61.7 |
| D | 30% | 锌片 | 79.9 |
第①组对照实验AC,变量硫酸的浓度(或质量分数);
第②组对照实验AB或CD,变量锌粒的形状.
【获得结论】
分析表中数据,可以得出的结论是硫酸的质量分数越大,反应速率越快;锌与硫酸的接触面积越大,反应速率越快;
【实验反思】
锌与硫酸溶液反应的快慢还可能受哪些因素影响?设计实验验证之.温度,取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间(只要有控制变量的意识即可).

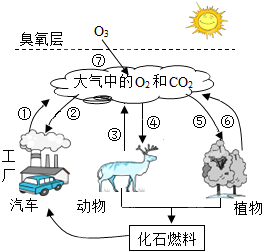 如图所示是自然界中氧气和二氧化碳的循环简图,请仔细读图,回答下列问题:
如图所示是自然界中氧气和二氧化碳的循环简图,请仔细读图,回答下列问题: