题目内容
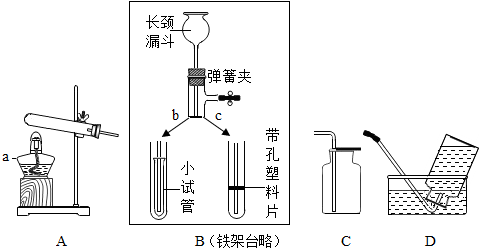
7.已知过氧化钠(化学式为Na2O2)是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂,利用人呼出的二氧化碳与过氧化钠反应放出氧气,供给人的正常生命活动,该反应的化学方程式为2Na2O2+2CO2═2Na2CO3+O2.某同学利用该反应原理制取氧气,设计实验装置如图所示:
(1)装置①中CO2的制取方法有多种:实验室制取CO2所用的药品是大理石(或石灰石)、稀盐酸.若用加热NaHCO3固体制取CO2,应该选用的发生装置为A(选填图2中字母),选取的依据是反应物是固体,且需要加热;
(2)假如要用装置③检验从装置②中出来的气体中有无CO2,装置③盛装的试剂你会选择澄清的石灰水,现象是澄清的石灰水变浑浊;
(3)④为O2的收集装置,可选用装置C(或E)(填字母序号);
(4)如图3实验装置,你会看到的现象是:下层的蜡烛先熄灭,上层的蜡烛后熄灭,从中反映出CO2的性质有二氧化碳不能燃烧、不支持燃烧,密度比空气大.
分析 (1)实验室制取二氧化碳用大理石或石灰石与稀盐酸混合,加热NaHCO3固体制取CO2,属于固体加热型,故选发生装置A;
(2)检验二氧化碳用澄清的石灰水,澄清的石灰水遇二氧化碳变浑浊;
(3)氧气难溶于水且密度比空气大,所以可以选择排水法或是向上排空气法来收集,可以据此选择装置;
(4)二氧化碳不能燃烧、不能支持燃烧、密度比空气大,据此分析解答.
解答 解:(1)实验室制取二氧化碳的药品是大理石或石灰石与稀盐酸,碳酸氢钠在加热的条件下分解产生二氧化碳,反应物是固体且需要加热,属于固体加热型,故选发生装置A;
(2)检验二氧化碳用澄清的石灰水,澄清的石灰水遇二氧化碳变浑浊;
(3)氧气不易溶于水且密度比空气大,所以可以选择排水法或向上排空气法来收集,故可用C或E收集;
(4)向烧杯内倒入二氧化碳,会观察到下层的蜡烛先熄灭,上层的蜡烛后熄灭,由此可知二氧化碳不能燃烧、不能支持燃烧、密度比空气大;
故答案为:(1)大理石(或石灰石)、稀盐酸;A;反应物是固体,且需要加热;
(2)澄清的石灰水;澄清的石灰水变浑浊;
(3)C(或E);
(4)下层的蜡烛先熄灭,上层的蜡烛后熄灭;二氧化碳不能燃烧、不支持燃烧,密度比空气大.
点评 本题考查了实验室制取二氧化碳的药品、二氧化碳的性质、装置选取,了解相关知识才能结合题意灵活解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15. 在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
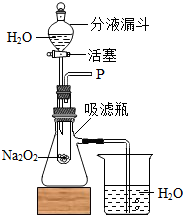
【设计装置]如图所示
【实验探究】
实验一:探究反应后生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:反应放出热量,吸滤瓶中的空气受热膨胀,从导管逸出.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.为了证实小军的看法,请你设计一个证明Na2CO3不存在的实验:
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现试管中的溶液变成红色,说明反应后所得的溶液呈碱性.
【表达】小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑.
 在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
【设计装置]如图所示
【实验探究】
实验一:探究反应后生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:反应放出热量,吸滤瓶中的空气受热膨胀,从导管逸出.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.为了证实小军的看法,请你设计一个证明Na2CO3不存在的实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量反应后的溶液于一试管中,向试管中滴加适量的稀盐酸 | 不产生气泡 | 生成物中没有Na2CO3 |
【表达】小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑.
2.建立宏观和微观之间的联系是化学学科特有的思维方式.下列对宏观事实的微观解释错误的是( )
| A. | 缉毒犬能根据气味发现毒品,是因为分子在不断运动 | |
| B. | 10mL酒精和10mL 水混合后体积小于20mL,是因为分子变小了 | |
| C. | 不同酸的化学性质有所不同,是因为解离生成的酸根离子不同 | |
| D. | 水电解生成氢气和氧气,是因为分子在化学变化中可以改变 |
12.下列除去杂质的方法中,正确的是( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO气体 | CO2气体 | 通过足量的 氢氧化钠溶液 |
| B | NaOH溶液 | Na2CO3 | 加入足量的 稀盐酸至不再产生气泡 |
| C | CaO固体 | CaCO3 | 加水溶解,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量锌粒,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |