题目内容
12.已知硫酸铜的化学式为CuSO4.试计算:(1)硫酸铜中铜原子、硫原子和氧原子的原子个数比为1:1:4.
(2)硫酸铜中铜元素和氧元素的质量比为1:1.
(3)硫酸铜的化学式量为160.
(4)硫酸铜中铜元素的质量分数为40%.
分析 (1)根据化学式的含义分析;
(2)据元素质量比=相对原子质量与相应原子个数的乘积比,及硫酸铜的化学式分析解答.
(3)利用相对分子质量为各元素相对原子质量的和即可求得硫酸铜的式量;
(4)纯净物中某元素的质量分数=$\frac{元素的相对原子质量×原子个数}{相对分子质量}$×100%,进行分析.
解答 解:(1)硫酸铜中铜原子、硫原子和氧原子的原子个数比为1:1:4,故填:1:1:4;
(2)在CuSO4中铜元素、氧元素的质量比为:64:(16×4)=1:1,故填:1:1;
(3)硫酸铜的化学式量为64+32+16×4=160;故填:160;
(4)硫酸铜中铜元素的质量分数=$\frac{64}{160}$×100%=40%;故填:40%;
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
2. 下面关于电解水的实验,说法正确的是( )
下面关于电解水的实验,说法正确的是( )
 下面关于电解水的实验,说法正确的是( )
下面关于电解水的实验,说法正确的是( )| A. | 实验说明水是由氢、氧两种元素组成 | |
| B. | 实验说明水是由氢气和氧气组成 | |
| C. | 水电解生成氢气和氧气的反应属于化合反应 | |
| D. | 若a试管中生成的气体为5mL则b试管中生成的气体为10mL |
20.“超临界水”因具有许多优良特质而被科学家追捧,它是指当气压和温度达到一定值时,水的液态和气态完全交融在一起的流体.下面有关“超临界水”说法正确的是( )
| A. | 它的分子之间有间隔 | |
| B. | 它是一种不同于水的物质 | |
| C. | 它是混合物 | |
| D. | 它的一个分子由4个氢原子和2个氧原子构成 |
4.为了测定实验室中氯酸钾样品的纯度,某学习小组取2.70克该样品与0.90克二氧化锰混合.加热该混合物时间后(假设杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t1,t2,t3,t4时间后剩余固体的质量,记录数据如下表
请仔细分析实验数据,回答下列问题:
(1)在t3时间后,该样品中的氯酸钾已经反应完全.
(2)求完全反应后产生氧气的质量.
(3)求该样品中氯酸钾的质量.
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量/g | 2.70 | 2.22 | 1.74 | 1.74 |
(1)在t3时间后,该样品中的氯酸钾已经反应完全.
(2)求完全反应后产生氧气的质量.
(3)求该样品中氯酸钾的质量.
15.请用适合的化学符号填空:
①2个氢原子2H;②氦气He;③海水中含量最多的金属元素Na;
④+3价的铝元素$\stackrel{+3}{Al}$;⑤铁离子Fe3+;⑥相对分子质量最小的氧化物H2O.
①2个氢原子2H;②氦气He;③海水中含量最多的金属元素Na;
④+3价的铝元素$\stackrel{+3}{Al}$;⑤铁离子Fe3+;⑥相对分子质量最小的氧化物H2O.
16. 在CO2复习课上,小组合作激发了师生学习的热情:
在CO2复习课上,小组合作激发了师生学习的热情:
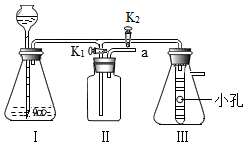
(一)老师设计了如图所示的实验装置,既可用于制取CO2,又可用于探究CO2性质.
说明:
1、装置Ⅰ中盛放的药品是石灰石和稀盐酸.
2、装置Ⅲ中在小试管外壁贴有4片试纸:其中两端的两片用紫色石蕊溶液润湿,中间两片用紫色石蕊溶液浸过并晒干.
(1)实验时,打开K1,关闭K2,可用来制备CO2.Ⅰ中反应的化学式表达式为CaCO3+2HCl═CaCl2+H2O+CO2↑,检验Ⅱ中气体收集满的方法是将燃着的木条放至导管口a处,木条熄灭说明收集满.
(2)实验时,关闭K1,打开K2,可用于探究CO2的性质.实验时Ⅲ中出现的现象是干燥试纸无变化,湿润试纸由下至上依次变红,有关反应的化学式表达式为CO2+H2O═H2CO3,该实验说明CO2具有的性质是密度比空气大、能与水反应.
(二)同学们把一瓶CO2气体(排空气法收集,并已验满)倒扣在盛水的水槽中,有的小组没有观察到水压入瓶中,有的小组观察到少量水压入瓶中.针对课堂中出现的现象,化学小组的同学在课外进行了探究.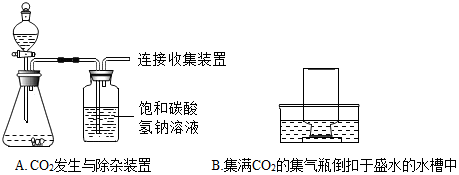
【提出问题】按教材的说法“1体积水大约能溶解1体积CO2”,水槽中的水足够把集气瓶中的CO2气体全部溶解,为什么集气瓶中的水面不上升或上升很少呢?
【作出猜想】
1、排空气法收集到的CO2气体可能不纯.
2、CO2溶于水需要时间较长.
3、…
【进行实验】小组同学分别用排空气法和排水法各收集2瓶CO2,重复图B实验,在不同时间测得压入的水量占集气瓶容积的百分数,数据见表1.
(已知:CO2在饱和碳酸氢钠溶液中溶解度很小)
表1 24小时内CO2溶解情况
【得出结论】
课堂中同学们没有观察到预期实验现象的原因是时间短,排空气法收集的气体不纯.
【实验反思】
该实验引发了同学们对向上排空气法收集CO2的纯度及CO2收集方法的思考.
(1)向上排空气法收集CO2的纯度.
小组同学用容积为150mL 的集气瓶,装入部分水,留一定量的空气,用CO2排出这些水.用此法收集到占空气体积分数不同的CO2气体,再将燃着的木条伸入集气瓶中,观察是否熄灭.试验不同浓度的CO2使燃着的木条熄灭的情况,实验结果见表 2.
表2 占空气体积分数不同的CO2使燃着的木条熄灭情况
上表中X的值为28%.
(2)排水法和向上排空气法收集气体所需时间对照
小组同学分4组用排水法和排空气法分别收集1瓶(集气瓶容积相同)CO2气体,记录所需时间,如表3所示.
表3 排水法和向上排空气法收集1瓶气体所需时间对照
①每次收集气体时,需要反应开始一段时间后再收集,其原因是排出装置内的空气.
②综合上述实验,请你对CO2的两种收集方法做出评价:排水法比排空气法收集的气体纯度高且收集时间短.
 在CO2复习课上,小组合作激发了师生学习的热情:
在CO2复习课上,小组合作激发了师生学习的热情:(一)老师设计了如图所示的实验装置,既可用于制取CO2,又可用于探究CO2性质.
说明:
1、装置Ⅰ中盛放的药品是石灰石和稀盐酸.
2、装置Ⅲ中在小试管外壁贴有4片试纸:其中两端的两片用紫色石蕊溶液润湿,中间两片用紫色石蕊溶液浸过并晒干.
(1)实验时,打开K1,关闭K2,可用来制备CO2.Ⅰ中反应的化学式表达式为CaCO3+2HCl═CaCl2+H2O+CO2↑,检验Ⅱ中气体收集满的方法是将燃着的木条放至导管口a处,木条熄灭说明收集满.
(2)实验时,关闭K1,打开K2,可用于探究CO2的性质.实验时Ⅲ中出现的现象是干燥试纸无变化,湿润试纸由下至上依次变红,有关反应的化学式表达式为CO2+H2O═H2CO3,该实验说明CO2具有的性质是密度比空气大、能与水反应.
(二)同学们把一瓶CO2气体(排空气法收集,并已验满)倒扣在盛水的水槽中,有的小组没有观察到水压入瓶中,有的小组观察到少量水压入瓶中.针对课堂中出现的现象,化学小组的同学在课外进行了探究.

【提出问题】按教材的说法“1体积水大约能溶解1体积CO2”,水槽中的水足够把集气瓶中的CO2气体全部溶解,为什么集气瓶中的水面不上升或上升很少呢?
【作出猜想】
1、排空气法收集到的CO2气体可能不纯.
2、CO2溶于水需要时间较长.
3、…
【进行实验】小组同学分别用排空气法和排水法各收集2瓶CO2,重复图B实验,在不同时间测得压入的水量占集气瓶容积的百分数,数据见表1.
(已知:CO2在饱和碳酸氢钠溶液中溶解度很小)
表1 24小时内CO2溶解情况
| 气体样本 | 1 | 2 | 3 | 4 |
| 收集方法 | 向上排空气法 | 向上排空气法 | 排水法 | 排水法 |
| 2小时 | 13.7% | 15.0% | 15.3% | 15.1% |
| 24小时 | 35.7% | 56.3% | 94.2% | 93.6% |
课堂中同学们没有观察到预期实验现象的原因是时间短,排空气法收集的气体不纯.
【实验反思】
该实验引发了同学们对向上排空气法收集CO2的纯度及CO2收集方法的思考.
(1)向上排空气法收集CO2的纯度.
小组同学用容积为150mL 的集气瓶,装入部分水,留一定量的空气,用CO2排出这些水.用此法收集到占空气体积分数不同的CO2气体,再将燃着的木条伸入集气瓶中,观察是否熄灭.试验不同浓度的CO2使燃着的木条熄灭的情况,实验结果见表 2.
表2 占空气体积分数不同的CO2使燃着的木条熄灭情况
| 实验1 | 实验2 | 实验3 | 实验4 | |
| 集气瓶中预留水的体积 | 60mL | 45mL | 42mL | 39mL |
| CO2的体积分数 | 40% | 30% | X | 26% |
| 燃着的木条状况 | 灭 | 灭 | 灭 | 不灭 |
(2)排水法和向上排空气法收集气体所需时间对照
小组同学分4组用排水法和排空气法分别收集1瓶(集气瓶容积相同)CO2气体,记录所需时间,如表3所示.
表3 排水法和向上排空气法收集1瓶气体所需时间对照
| 1 | 2 | 3 | 4 | |
| 排水法 | 35“ | 43“ | 43“ | 43“ |
| 排空气法 | 1'57“ | 1'15“ | 1'4“ | 1'12“ |
②综合上述实验,请你对CO2的两种收集方法做出评价:排水法比排空气法收集的气体纯度高且收集时间短.
 如图为某元素的原子结构示意图,请据此回答:
如图为某元素的原子结构示意图,请据此回答:
 己知A、B、C、D是初中化学中四种常见的物质,A是可供给呼吸的气体,D可用于常温下制取A,B、C的组成元素相同,它们之间存在如图的反应与转化关系(图中“→”表示转化关系)
己知A、B、C、D是初中化学中四种常见的物质,A是可供给呼吸的气体,D可用于常温下制取A,B、C的组成元素相同,它们之间存在如图的反应与转化关系(图中“→”表示转化关系)