题目内容
(2011?威海)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤液47.67g.请你通过计算,求出氢氧化钡溶液的溶质质量分数.可能用到的相对原子质量:H-1 O-16 S-32 Ba-137.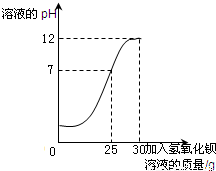
【答案】分析:本题涉及的反应为,图象为反应后溶液的pH随加入氢氧化钡溶液加入而变化的情况.根据图象可知,当加入25g氢氧化钡溶液时,与稀硫酸恰好完全中和,此后所加氢氧化钡溶液不再发生反应,因此,根据质量质量定律可计算加入25g氢氧化钡溶液恰好完全反应时生成沉淀的质量;利用沉淀硫酸钡的质量,根据反应的化学方程式,计算出25g氢氧化钡溶液中溶质氢氧化钡的质量,最后使用溶液中溶质质量分数公式计算氢氧化钡溶液的溶质质量分数.
解答:解:根据质量守恒定律,生成的BaSO4质量为:20g+30g-47.67g=2.33g;
设参加反应的Ba(OH)2的质量为x
Ba(OH)2+H2SO4=BaSO4↓+2H2O
171 233
x 2.33g
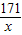 =
= x=1.71g
x=1.71g
而在滴入氢氧化钡溶液25g时是恰好完全反应的(这一点不影响沉淀的最后称量,因为沉淀不再生成),所以生成2.33g沉淀时需要的1.71g的氢氧化钡来自于25g的氢氧化钡溶液.
Ba(OH)2的溶质质量分数=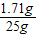 ×100%=6.84%
×100%=6.84%
答:该溶液中Ba(OH)2的溶质质量分数为6.84%.
点评:根据质量守恒定律,生成沉淀硫酸钡的质量=稀硫酸的质量20g+所加入氢氧化钡溶液的质量30g-过滤后所得滤液的质量47.67g.
解答:解:根据质量守恒定律,生成的BaSO4质量为:20g+30g-47.67g=2.33g;
设参加反应的Ba(OH)2的质量为x
Ba(OH)2+H2SO4=BaSO4↓+2H2O
171 233
x 2.33g
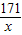 =
= x=1.71g
x=1.71g而在滴入氢氧化钡溶液25g时是恰好完全反应的(这一点不影响沉淀的最后称量,因为沉淀不再生成),所以生成2.33g沉淀时需要的1.71g的氢氧化钡来自于25g的氢氧化钡溶液.
Ba(OH)2的溶质质量分数=
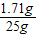 ×100%=6.84%
×100%=6.84%答:该溶液中Ba(OH)2的溶质质量分数为6.84%.
点评:根据质量守恒定律,生成沉淀硫酸钡的质量=稀硫酸的质量20g+所加入氢氧化钡溶液的质量30g-过滤后所得滤液的质量47.67g.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(2011?威海)化学与环境保护--探究酸雨的腐蚀性:
我国道教发源地山东威海圣经山摩崖石刻,为国内罕见的大型道教石刻,可称为瑰宝.圣经山摩崖石刻的材质是大理石,主要成分是碳酸钙,现在字迹已模糊不清.摩崖石刻被腐蚀,是否是酸雨所致?试回答下列问题:
(1)酸雨的成因:即使大气没有受到污染,正常的雨水或河水也呈微弱酸性(pH在5.6~7之间),原因是______.酸雨的酸性比正常雨水强,是因为雨水吸收了被污染的大气中的______等有害气体.大气中这些有害气体主要来自于______.
(2)定量实验探究:
查阅资料及定性实验表明:①醋酸和酸雨的酸性程度差不多,pH在5.6~3之间;②酸雨(醋酸)确实能加重大理石腐蚀的程度.③定性实验显示:将大理石放入pH=3的醋酸溶液中,短时间内几乎看不出有气泡产生.
现提供下列仪器和试剂:
仪器:烧杯、托盘天平、镊子、量筒、胶头滴管.
药品:pH=6.5的普通雨水、pH=3醋酸溶液、大理石薄片.
请你设计一个“定量实验方案”,证明摩崖石刻被腐蚀,主要与酸雨有关,与普通雨水无关.
(3)下列与保护摩崖石刻有关的说法中,你同意的是______
A.了解哪种人类活动最容易引起酸雨
B.引起酸雨原因的结论应建立在科学研究的基础上
C.保护摩崖石刻要建立在有关损坏原因的科学证据的基础上
D.要从根本上预防酸雨的危害,应禁止工厂和汽车排放气体
E.要减少酸雨的危害,应研究和推广减少有害气体排放的技术
F.要从根本上保护摩崖石刻,主要应研究修复被酸雨损伤的摩崖石刻的方法与技术.
我国道教发源地山东威海圣经山摩崖石刻,为国内罕见的大型道教石刻,可称为瑰宝.圣经山摩崖石刻的材质是大理石,主要成分是碳酸钙,现在字迹已模糊不清.摩崖石刻被腐蚀,是否是酸雨所致?试回答下列问题:
(1)酸雨的成因:即使大气没有受到污染,正常的雨水或河水也呈微弱酸性(pH在5.6~7之间),原因是______.酸雨的酸性比正常雨水强,是因为雨水吸收了被污染的大气中的______等有害气体.大气中这些有害气体主要来自于______.
(2)定量实验探究:
查阅资料及定性实验表明:①醋酸和酸雨的酸性程度差不多,pH在5.6~3之间;②酸雨(醋酸)确实能加重大理石腐蚀的程度.③定性实验显示:将大理石放入pH=3的醋酸溶液中,短时间内几乎看不出有气泡产生.
现提供下列仪器和试剂:
仪器:烧杯、托盘天平、镊子、量筒、胶头滴管.
药品:pH=6.5的普通雨水、pH=3醋酸溶液、大理石薄片.
请你设计一个“定量实验方案”,证明摩崖石刻被腐蚀,主要与酸雨有关,与普通雨水无关.
| 实验内容及步骤 | 应得到的实验结果 |
A.了解哪种人类活动最容易引起酸雨
B.引起酸雨原因的结论应建立在科学研究的基础上
C.保护摩崖石刻要建立在有关损坏原因的科学证据的基础上
D.要从根本上预防酸雨的危害,应禁止工厂和汽车排放气体
E.要减少酸雨的危害,应研究和推广减少有害气体排放的技术
F.要从根本上保护摩崖石刻,主要应研究修复被酸雨损伤的摩崖石刻的方法与技术.