题目内容
13.标出下列各组物质中加点元素的化合价:(1)H2S-2 S0 SO2+4 Na2SO3+4 H2SO4+6
(2)MnO2+4 MnCl2+2 Mn0 KMnO4+7 K2MnO4+6.
分析 根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,结合各化学式计算出化合价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,进行分析解答.
解答 解:(1)氢元素显+1价,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x=0,则x=-2价;根据单质中元素的化合价为0,S属于单质,故硫元素的化合价为0;氧元素显-2价,设硫元素的化合价是y,可得:y+(-2)×2=0,则y=+4价;钠元素显+1价,氧元素显-2价,设硫元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)×2+z+(-2)×3=0,则z=+4价;氢元素显+1价,氧元素显-2价,设硫元素的化合价是m,根据在化合物中正负化合价代数和为零,可得:(+1)×2+m+(-2)×4=0,则m=+6价;.
故填:-2;0;+4;+4;+6.
(2)氧显-2价,氯显-1价,钾显+1价,根据单质中元素的化合价为0、在化合物中正负化合价代数和为零可知,二氧化锰、氯化锰、锰、高锰酸钾、锰酸钾中锰元素的化合价分别为+4、+2、0、+7、+6,故填:+4;+2;0;+7;+6.
点评 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答本题.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
10.图为初中化学常见气体的发生与收集装置.有关这些装置用途的说法正确的是( )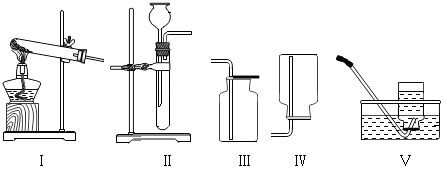

| A. | 装置Ⅰ可作为固液加热制取气体的发生装置 | |
| B. | 通常采用热胀冷缩的原理检验装置Ⅱ的气密性 | |
| C. | 装置Ⅰ和Ⅴ组合可用于制取O2 | |
| D. | 装置Ⅱ和Ⅲ组合可用于制取H2 |
1.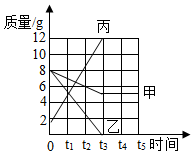 在一密闭容器中,甲乙丙三种物质在一定条件下充分反应,反应前后各物质的质量变化如图所示.下列说法正确的是( )
在一密闭容器中,甲乙丙三种物质在一定条件下充分反应,反应前后各物质的质量变化如图所示.下列说法正确的是( )
 在一密闭容器中,甲乙丙三种物质在一定条件下充分反应,反应前后各物质的质量变化如图所示.下列说法正确的是( )
在一密闭容器中,甲乙丙三种物质在一定条件下充分反应,反应前后各物质的质量变化如图所示.下列说法正确的是( )| A. | 该反应为分解反应 | |
| B. | 参加反应的各物质的总质量为17g | |
| C. | 反应中的甲和丙两物质的质量比为1:8 | |
| D. | 该反应可能是碳和氧气充分反应 |
8.下列变化中,属于化学变化,并且能用质量守恒定律解释的是( )
| A. | 5 g水受热变成5 g水蒸气 | |
| B. | 5 g食盐溶解在95 g水中,成为100 g食盐溶液 | |
| C. | 100 mL水加入100 mL酒精,体积小于200 mL | |
| D. | 木炭燃烧后质量减少 |
2.有X、Y、Z三种金属,将X、Y、Z分别加入到相同的稀盐酸溶液中,只有Y表面产生气泡,另将X加入到Z的硝酸盐溶液中,无明显现象产生,由此判断金属活动性顺序正确的是( )
| A. | X>Y>Z | B. | Y>Z>X | C. | Y>X>Z | D. | Z>Y>X |
