题目内容
14.某固体混合物由Mg和MgO组成,取该混合物6.4g与一定量稀硫酸恰好完全反应(反应后溶液中无晶体析出),所得溶液中溶质的质量为24g,则原混合物中氧元素的质量为( )| A. | 4.8g | B. | 3.2g | C. | 1.6g | D. | 2.56g |
分析 根据化学反应原理知所得溶液的溶质为MgSO4,根据元素守恒定律知硫酸镁中镁元素的质量即为原固体混合物中镁元素的质量,混合物的质量减去镁元素的质量即为氧元素的质量;
解答 解:镁粉和氧化镁与硫酸反应的化学方程式为Mg+H2SO4=MgSO4+H2↑;MgO+H2SO4=MgSO4+H2O;
由此可推出所得24g为硫酸镁的质量,
硫酸镁中镁元素的质量为24g×$\frac{24}{24+96}$×100%=4.8g;硫酸镁中镁元素的质量即为混合物中镁元素的质量.
混合物中氧元素的质量即为:6.4g-4.8g=1.6g.
答案:C.
点评 解答本题主要是利用元素质量守恒定律进行解答.这在解多步反应计算或混合物计算中可以省略中间步骤,加快解题速度

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
4.有A、B、C、D四种原子,已知它们的核电荷数依次增大且为四个连续的数.B和D的原子核里质子数和中子数相等,A和C的原子核里质子数比中子数少1,已知B原子核外有10个电子.
(1)根据以上事实填写下表:
(2)分析表中的数据,你发现了哪些规律?①质子数=核电荷数=核外电子数②质子数不一定等于中子数.
(1)根据以上事实填写下表:
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 核电荷数 |
| A | ||||
| B | 10 | |||
| C | ||||
| D |
9.下列不可以作为气体干燥剂的是( )
| A. | 浓硫酸 | B. | 石灰石 | C. | 氢氧化钠固体 | D. | 生石灰 |
19.下列物质的用途,由物理性质决定的是( )
| A. | 食醋用于清除水壶中的水垢 | B. | 浓硫酸做某些气体的干燥剂 | ||
| C. | 二氧化碳作气体肥料 | D. | 用镁做军事照明弹 |
3.物质的性质决定其用途.下列物质的用途与性质对应关系错误的是( )
| A. | 氢气用作燃料----氢气具有可燃性 | |
| B. | 氧化钙作食品干燥剂----氧化钙能与水反应 | |
| C. | 氮气用作保护气----氮气化学性质稳定 | |
| D. | 干冰用于人工降雨----二氧化碳能与碱反应 |
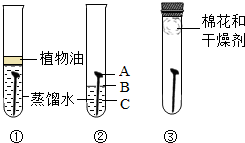 某学习小组用相同的光亮铁钉探究生锈与哪些因素有关,设计的实验如图所示:
某学习小组用相同的光亮铁钉探究生锈与哪些因素有关,设计的实验如图所示: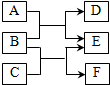 物质A~F都是初中化学中的常见物质,它们有如图所示的转化关系.请回答下列问题(反应条件已略):
物质A~F都是初中化学中的常见物质,它们有如图所示的转化关系.请回答下列问题(反应条件已略):