��Ŀ����
�±���KNO3 ��NaCl�ڲ�ͬ�¶��µIJ����ܽ�����ݣ���λ��g/100gˮ������ش����⣺
|
�¶ȣ��棩 |
10 |
20 |
40 |
60 |
80 |
|
KNO3 |
20.9 |
31.6 |
63.9 |
110 |
169 |
|
NaCl |
35.8 |
36 |
36.6 |
37.3 |
38.4 |
��1��10��ʱ��KNO3 �ܽ���� g/100gˮ��
��2���������������ܽ�ȱ仯���¶�Ӱ���С���� ��
��3��40��ʱ����70gKNO3�������100gˮ�У���ֽ��裬�γɵ���Һ����Ϊ g��
��4��60��ʱ��KNO3�ı�����Һ�к�������NaCl��ͨ�� ������ýϴ�����KNO3���塣
��5�����ݱ������ݣ���������ͼ����㡢���Ʒ���KNO3�ܽ�ȱ仯���ɵ����� ��

��6����20mLˮ���ܽ�һ����KNO3����IJ�������ͼ�������ʵ��������ܽ�����ݻش�A��B��C��
��Һһ���DZ�����Һ���� ��һ���Dz�������Һ���� ����x = g
ʱ��B��ǡ��û�й���ʣ�ࡣ

��1��20.9 ��2��NaCl ��3��163.9 ��4����ȴ������Һ�����£���5���������ȷ��1�֣����߹⻬��������ȷ��1�֣������⻬�������߿�1�֣�ԭ�������1��
��6��B A 1.32
��������
����������ɱ�����Ϣ��֪��10��ʱKNO3 �ܽ����g/100gˮ��
�������������ܽ�ȱ仯���¶�Ӱ���С�����Ȼ��ơ�
40��ʱ��KNO3 �ܽ����63.9g������70gû����ȫ�ܽ⣬��Һ����=���ʣ��ܽ�ģ�����+�ܼ�����=63.9g+100g=163.9g��
�ᾧ�ķ��������֣�����ȴ������Һ���÷���Ӧ���ܽ�����¶�Ӱ���ģ�������أ��������ܼ������÷���Ӧ���ܽ�����¶�Ӱ��С�ģ����Ȼ��ơ���KNO3�ı�����Һ�к�������NaCl��ͨ����ȴ������Һ������ýϴ�����KNO3���塣
���ձ��и������¶�����ͼ��
���㣺�����ܽ�����������ã�������Һ�Ͳ�������Һ�����ʵ������������ܽ��Ժ��ܽ�ȵĹ�ϵ��

������Ϣ�ش����⣺
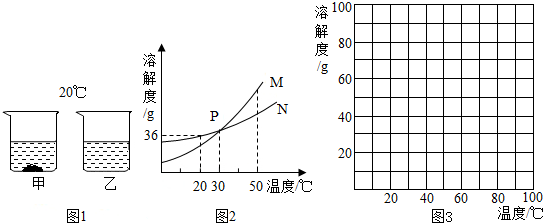
��1��20��ʱ�����������ļס������ֹ������ʣ��ֱ���뵽ʢ��100gˮ���ձ��У���ֽ����������ͼ1���ס������ֹ��������ܽ��������ͼ2�����ͼʾ�ش��������⣺

��______��ʱ�������ʵ��ܽ����ȣ�
��ͼ2�б�ʾ�ҵ��ܽ��������______��
��20��ʱ��19g����N�ܽ���50gˮ��������Һ��Ũ����______����ȷ��0.1%����
��2���±���NaCl��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ�
| �¶ȣ��棩 | 0 | 10 | 20 | 40 | 50 | 60 | 70 |
| KNO3 | 13.3 | 20.9 | 31.6 | 64 | 85.5 | 110 | 138 |
| NaCl | 35.7 | 35.8 | 36 | 36.6 | 37 | 37.5 | 37.8 |
����ͨ�����µķ�����NaCl��KNO3�Ļ����Һ���ᴿKNO3��ʣ����Һ�������ľ���������ȷ����______��
A��ʣ����Һһ����KNO3������Һ
B��ʣ����Һһ����NaCl��������Һ
C�������������Խ�������ȫ����
D�������ľ�����ֻ����KNO3
����һ���¶��£�����69g KNO3��18g NaCl�Ļ������ȫ�ܽ���50gˮ�У��ı��¶�ʹKNO3������NaCl�����������¶ȷ�Χ��______������غ��Ȼ����ܽ�Ȼ���Ӱ�죩��


 �����±��ش����⣮
�����±��ش����⣮