题目内容
根据信息回答问题:
(1)20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,甲、乙两种固体物质溶解度曲线如图2,结合图示回答下列问题:
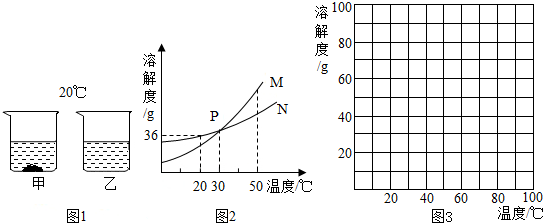
① ℃时两种物质的溶解度相等.
②图2中表示乙的溶解度曲线是 .
③20℃时将19g物质N溶解在50g水里所得溶液的浓度是 (精确到0.1%).
(2)下表是NaCl和KNO3在不同温度时的溶解度:
①在图3中画出硝酸钾0℃~40℃的溶解度曲线.
②若通过降温的方法从NaCl和KNO3的混合溶液中提纯KNO3后,对剩余溶液及析出的晶体描述正确的是 .
A.剩余溶液一定是KNO3饱和溶液
B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离
D.析出的晶体中只含有KNO3
③在一定温度下,将含69g KNO3、18g NaCl的混合物完全溶解在50g水中,改变温度使KNO3析出,NaCl不析出,则温度范围是 (硝酸钾和氯化钠溶解度互不影响).
(1)20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,甲、乙两种固体物质溶解度曲线如图2,结合图示回答下列问题:

①
②图2中表示乙的溶解度曲线是
③20℃时将19g物质N溶解在50g水里所得溶液的浓度是
(2)下表是NaCl和KNO3在不同温度时的溶解度:
| 温度(℃) | 0 | 10 | 20 | 40 | 50 | 60 | 70 |
| KNO3 | 13.3 | 20.9 | 31.6 | 64 | 85.5 | 110 | 138 |
| NaCl | 35.7 | 35.8 | 36 | 36.6 | 37 | 37.5 | 37.8 |
②若通过降温的方法从NaCl和KNO3的混合溶液中提纯KNO3后,对剩余溶液及析出的晶体描述正确的是
A.剩余溶液一定是KNO3饱和溶液
B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离
D.析出的晶体中只含有KNO3
③在一定温度下,将含69g KNO3、18g NaCl的混合物完全溶解在50g水中,改变温度使KNO3析出,NaCl不析出,则温度范围是
分析:(1)①溶解度曲线的交点表示该温度下两物质的溶解度相等;
②根据图1信息可以知道20℃时甲的溶解度小于乙的溶解度,结合图2可以完成解答;
③据20℃时N的溶解度分析解答;
(2)①根据图表中硝酸钾在不同温度下的溶解度绘制其溶解度曲线;
②根据饱和溶液的含义及题意分析解答;
③根据硝酸钾和氯化钠的溶解度进行解答.
②根据图1信息可以知道20℃时甲的溶解度小于乙的溶解度,结合图2可以完成解答;
③据20℃时N的溶解度分析解答;
(2)①根据图表中硝酸钾在不同温度下的溶解度绘制其溶解度曲线;
②根据饱和溶液的含义及题意分析解答;
③根据硝酸钾和氯化钠的溶解度进行解答.
解答:解:(1)①由于在30℃时,两物质的溶解度曲线交于一点,即两物质的溶解度相等;
②由图1可知,在20℃时,100克水中溶解的乙物质多,即乙的溶解度大,因此N代表的是乙,M代表的是甲;
③20℃时N的溶解度是36g,故20℃时将19g物质N溶解在50g水里最多溶解18g,所得溶液的浓度是
×100%≈26.5%;
(3)①根据硝酸钾在0℃~40℃的溶解度绘制其溶解度曲线,见下图;
②饱和溶液是指在一定温度下,不能再溶解这种溶质的溶液,既然有晶体析出,剩余的溶液一定是硝酸钾的饱和溶液;但不一定是氯化钠的饱和溶液,但该方法不能将两物质完全分离,析出的晶体中可能含有氯化钠,故选A;
③在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中.改变温度使KNO3析出,NaCl不析出,根据氯化钠的溶解度可知,18gNaCl的混合物完全溶解在50g水中氯化钠不析出,温度应该大于或等于20℃,69gKNO3溶解在50g水中使KNO3析出,温度应该不高于70℃,所以温度T(℃)的范围是20℃~70℃;
故答案为:(1)①30;②N;③26.5%;
(2)①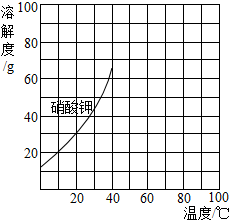 ②A;③20℃~70℃.
②A;③20℃~70℃.
②由图1可知,在20℃时,100克水中溶解的乙物质多,即乙的溶解度大,因此N代表的是乙,M代表的是甲;
③20℃时N的溶解度是36g,故20℃时将19g物质N溶解在50g水里最多溶解18g,所得溶液的浓度是
| 18g |
| 68g |
(3)①根据硝酸钾在0℃~40℃的溶解度绘制其溶解度曲线,见下图;
②饱和溶液是指在一定温度下,不能再溶解这种溶质的溶液,既然有晶体析出,剩余的溶液一定是硝酸钾的饱和溶液;但不一定是氯化钠的饱和溶液,但该方法不能将两物质完全分离,析出的晶体中可能含有氯化钠,故选A;
③在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中.改变温度使KNO3析出,NaCl不析出,根据氯化钠的溶解度可知,18gNaCl的混合物完全溶解在50g水中氯化钠不析出,温度应该大于或等于20℃,69gKNO3溶解在50g水中使KNO3析出,温度应该不高于70℃,所以温度T(℃)的范围是20℃~70℃;
故答案为:(1)①30;②N;③26.5%;
(2)①
 ②A;③20℃~70℃.
②A;③20℃~70℃.点评:解答这类题目时,首先要熟记和理解固体溶解度曲线及其使用,固体溶解度的概念和意义,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念,并按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
相关题目
 13、如图是钙元素在元素周期表中的相关信息及钙原子结构示意图,请根据信息回答问题:
13、如图是钙元素在元素周期表中的相关信息及钙原子结构示意图,请根据信息回答问题:
