题目内容
9. 天然水中一般都溶有Ca(HCO3)2、Mg(HCO3)2等物质,在加热条件下,这些溶解的物质会变成溶解度更小的碱和碳酸盐等其它物质,所以保温瓶中常会形成由碱和碳酸盐等组成的水垢.
天然水中一般都溶有Ca(HCO3)2、Mg(HCO3)2等物质,在加热条件下,这些溶解的物质会变成溶解度更小的碱和碳酸盐等其它物质,所以保温瓶中常会形成由碱和碳酸盐等组成的水垢.查阅资料,甲、乙、丙三位同学知道水垢中含有Mg(OH)2,和CaCO3后,提出了是否有Ca(OH)2和MgCO3的猜测.于是,进行下列研究.
(1)通过实验发现,水垢中不存在Ca(OH)2,他们采用的实验操作是在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入浓Na2C03溶液,没有白色沉淀产生.
(2)甲同学设计如图所示的装置,利用一定量的水垢与足量的稀盐酸反应,待产生气泡停止后,测量B装置增加的质量,从而推出混合物的组成.这种方案受到乙、丙同学的反对,他们的理由是此装置不能充分吸收生成的CO2,且通入B装置的气体是C02、水蒸气等混合气体.
(3)甲改进装置后,利用正确的方法测得5克水垢与足量的稀盐酸反应后,放出2.2克CO2,说明有(填“有”或“没有”)MgCO3.
分析 (1)根据碳酸钠和氢氧化钙反应生成碳酸钙沉淀进行分析;
(2)根据装置内的二氧化碳不能被氢氧化钠充分吸收、氢氧化钠进行分析;
(3)根据碳酸钙、碳酸镁和盐酸反应生成二氧化碳的方程式进行计算.
解答 解:(1)碳酸钠和氢氧化钙反应生成碳酸钙沉淀,所以通过实验发现,水垢中不存在Ca(OH)2,采用的实验操作是:在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入浓Na2C03溶液,没有白色沉淀产生;
(2)甲同学设计如图所示的装置,利用一定量的水垢与足量的稀盐酸反应,待产生气泡停止后,测量B装置增加的质量,从而推出混合物的组成.这种方案受到乙、丙同学的反对的理由是:此装置不能充分吸收生成的CO2,且通入B装置的气体是C02、水蒸气等混合气体;
(3)假设5g全部是碳酸钙,生成二氧化碳的质量为x
CaCO3----CO2,
100 44
5g x
$\frac{100}{5g}$=$\frac{44}{x}$
x=2.2g
假设5g全部是碳酸镁,生成二氧化碳的质量为y
MgCO3---------CO2,
84 44
5g y
$\frac{84}{5g}$=$\frac{44}{y}$
y=2.6g
甲、乙、丙三位同学知道水垢中含有Mg(OH)2,和CaCO3后,所以混合物中一定含有碳酸镁.
故答案为:(1)在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入浓Na2C03溶液,没有白色沉淀产生;
(2)此装置不能充分吸收生成的CO2,且通入B装置的气体是C02、水蒸气等混合气体;
(3)有.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.

【实验用品】pH试纸、Zn片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液
【假设猜想】猜想一:硫酸钠 猜想二:硫酸钠、碳酸氢钠 猜想三:硫酸钠、硫酸
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据现象或结论填空.
| 实验方案 | A | B | C | D |
| 实验操作 | 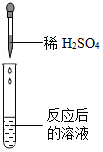 | 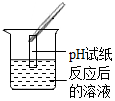 |  | 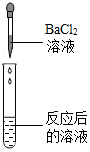 |
| 实验现象 | 无气泡产生 | 试纸变色对照比色卡,pH<7 | 产生气泡 | 产生白色沉淀 |
| 实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
【评价反思】老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在两处明显错误,分别是:
①方案B中pH试纸浸入溶液中;②方案D中硫酸钠和氯化钡反应也能够产生白色沉淀,不能证明溶液中含有硫酸.
【总结提高】依据所给实验用品,你还有什么不同类方案确认猜想三是正确的,请你写出你的实验方案取少量氧化铜粉末于试管中,加入足量反应后的溶液,若氧化铜溶解,溶液变蓝色,则猜想三正确.
| A. |  滴加盐酸 | B. |  滴加氯化铜溶液 | C. |  滴加无色酚酞 | D. |  通入二氧化碳 |
| A. | 自然沉淀法 | B. | 过滤法 | C. | 蒸馏法 | D. | 加凝聚剂沉淀法 |
| A. | CCl4和H2 | B. | CCl4和HCl | C. | CH3Cl和H2 | D. | CCl4和H2O |
| A. | 钻石(C) | B. | 水晶(SiO2) | C. | 食盐(NaCl) | D. | 钟乳石(CaCO3) |
