题目内容
18.甲、乙、丙、丁4种常见物质,由氢、碳、氧、钠、钙5种元素中的2-3种组成.(1)甲俗称纯碱,其化学式为Na2CO3,乙是一种氧化物,遇水放出大量的热,乙的俗称是生石灰,丙与氧气在点燃条件下反应,其微观示意图如图1,请在方框中补全相应微粒的图示.

(2)如图2所示(夹持仪器略去,K1、K2均关闭),打开K1,待液体全部流下,立即关闭K1,观察到产生大量气泡,且烧杯中丁的溶液变浑浊.充分反应后,打开K1和K2,使液体全部流入锥形瓶,瓶中无明显现象.取反应后锥形瓶中的溶液,测得pH=3,则该溶液中含有的溶质除HCl外,还有NaCl、CaCl2(填化学式).
分析 (1)碳酸钠俗称纯碱,写出化学式;根据氧化钙与水反应生成了氢氧化钙能放出大量的热分析回答;根据质量守恒定律反应前后原子的种类、数目不变分析;
(2)根据二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和和水,结合盐酸、碳酸钠、氢氧化钙的性质反应进行分析.
解答 解:(1)甲俗称纯碱,则甲为碳酸钠,化学式为Na2CO3;由于氧化钙与水反应生成了氢氧化钙能放出大量的热,氧化钙是由钙、氧两种元素组成的,属于氧化物,由此可知,乙的名称是氧化钙;由物质的微观构成可知,丙为甲烷,燃烧生成了二氧化碳和水,由质量守恒定律反应前后原子的种类、数目不变可知,在方框中补应补充两个水分子,见下图:
(2)由于盐酸与碳酸钠反应生成的二氧化碳能使氢氧化钙溶液变浑浊,氢氧化钙是由上述中的元素组成的,所以,丁物质是氢氧化钙;由题意可知,锥形瓶中的溶液的pH=3,说明溶液中有剩余的盐酸,则碳酸钠、氢氧化钙完全反应,该溶液中含有的溶质除HCl外,还有盐酸与碳酸钠、氢氧化钙生成的NaCl、CaCl2.
故答为:(1)Na2CO3;氧化钙; ;(2)NaCl、CaCl2.
;(2)NaCl、CaCl2.
点评 本题的推断由组成物质的元素做为限定条件,因此,熟悉常见物质的组成、性质及变化规律对该题中所涉及物质的推断就至关重要了.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
9.下列说法中正确的是( )
| A. | 红磷在氧气中能燃烧,在空气中不能燃烧 | |
| B. | 硫在氧气中燃烧后生成有刺激性气味的气体 | |
| C. | 镁条在氧气中燃烧时.火星四射,生成黑色固体 | |
| D. | 木炭伸入盛有氧气的集气瓶中剧烈燃烧,发出白光 |
6.节能减排、低碳出行是我们倡导的生活方式,“低碳”指的是尽量减少二氧化碳的排放.下列有关二氧化碳的说法正确的是( )
| A. | 二氧化碳通入紫色石蕊溶液,溶液变为红色,说明二氧化碳具有酸性 | |
| B. | 实验室中可用块状石灰石和稀硫酸反应制取二氧化碳气体 | |
| C. | 二氧化碳和一氧化碳的组成元素相同,在一定条件下可以相互转化 | |
| D. | 进入久未开启的菜窖之前,必须做灯火试验,是因为二氧化碳有毒 |
7.下列有关水的认识中正确的是( )
| A. | 地球水资源丰富,我们没有必要节约用水 | |
| B. | 长期饮用蒸馏水对身体健康没有好处 | |
| C. | 自然界中的水,过滤之后澄清透明,就成了软水 | |
| D. | 工业废水只要无色透明就可以直接饮用 |
8.下列化学方程式书写正确的是( )
| A. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | B. | Fe+O2$\frac{\underline{\;点燃\;}}{\;}$FeO2 | ||
| C. | 2H2O═2H2+O2 | D. | C+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2↑ |
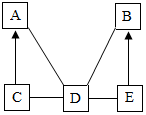 A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质,B在空气中易潮解,C是红棕色固体,E俗称纯碱,图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题:
A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质,B在空气中易潮解,C是红棕色固体,E俗称纯碱,图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题: