题目内容
下列各组离子中在水溶液中能大量共存的是( )
| A、Fe2+,Ca2+,CO32-,OH- |
| B、Na+,SO42-,Cl-,OH- |
| C、Ba2+,H+,Cl-,SO42- |
| D、Ag+,NH4+,NO3-,Cl- |
考点:离子或物质的共存问题
专题:物质的分离、除杂、提纯与共存问题
分析:复分解反应的条件:必须有水、沉淀或气体生成,即阴阳离子重新组合有水、沉淀或气体生成;离子在溶液中可以大量共存说明阴阳离子组合时没有水、沉淀或气体生成.
解答:解:A、由于Fe2+和OH-能生成氢氧化亚铁沉淀,CO32-和Ca2+生成碳酸钙沉淀,不能共存,故A错误;
B、由于阴阳离子组合时没有水、沉淀或气体生成,因此这四种离子在水溶液中可以大量共存,故B正确;
C、由于Ba2+和SO42-结合生成硫酸钡沉淀,不能共存,故C错误;
D、由于Ag+和Cl-结合生成氯化银沉淀,不能共存,故D错误.
故选项为:B.
B、由于阴阳离子组合时没有水、沉淀或气体生成,因此这四种离子在水溶液中可以大量共存,故B正确;
C、由于Ba2+和SO42-结合生成硫酸钡沉淀,不能共存,故C错误;
D、由于Ag+和Cl-结合生成氯化银沉淀,不能共存,故D错误.
故选项为:B.
点评:本题难度不是很大,主要考查了复分解反应的条件及其应用,只要生成沉淀、气体、水中的一种,就不能共存,能够培养学生解决问题的能力.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
学校安全无小事,下列做法可能造成安全事故的是( )
| A、扇闻气体的气味 |
| B、先预热,再给试管内的物质加热 |
| C、用灯帽盖灭酒精灯 |
| D、用手取固体药品 |
某物质在纯氧中燃烧生成了二氧化碳和水蒸气,该物质一定含有( )
| A、碳元素 |
| B、碳元素和氧元素 |
| C、碳元素和氢元素 |
| D、碳元素、氢元素和氧元素 |
 所示,则该原子的核电荷数为
所示,则该原子的核电荷数为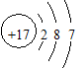 ,则它的电子数为
,则它的电子数为