题目内容
有一铁与氧化亚铁的混合物,其中铁元素的质量分数为80%,取该混合物7.0克,加足量稀硫酸完全反应,生成硫酸亚铁的质量为 克.
考点:混合物中某元素的质量计算,化合物中某元素的质量计算,质量守恒定律及其应用
专题:化学式的计算
分析:根据题意,一铁与氧化亚铁的混合物,其中铁元素的质量分数为80%,取该混合物7.0克,加足量稀硫酸完全反应生成硫酸亚铁,据此结合质量守恒定律反应前后元素种类不变、化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:一铁与氧化亚铁的混合物,其中铁元素的质量分数为80%,取该混合物7.0克,则混合物中铁元素的质量为7.0g×80%=5.6g;加足量稀硫酸完全反应生成硫酸亚铁,由质量守恒定律反应前后,元素种类不变,生成硫酸亚铁的质量为5.6g÷(
×100%)=15.2g
故答案为:15.2.
| 56 |
| 56+32+16×4 |
故答案为:15.2.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算、质量守恒定律等进行分析问题、解决问题的能力.

练习册系列答案
相关题目
没有化学科学的发展,就没有今日丰富多彩的世界.下列事实与化学没有密切联系的是( )
| A、新材料的研制 |
| B、“神十”飞天轨道的设定 |
| C、农药、化肥的研制 |
| D、新能源的开发和利用 |
下列厨房中的物质,放入一定量水中能形成的溶液的是( )
| A、食盐 | B、面粉 | C、花生油 | D、粉芡 |
下列物质的化学符号书写正确的是( )
| A、镁 mg |
| B、水 H2O |
| C、铝 AL |
| D、二氧化碳 CO2 |
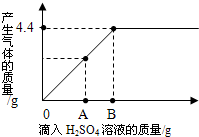 在一烧杯中盛20g Na2CO3和Na2SO4的白色固体混合物,向其中逐滴滴加溶质质量分数为10%的H2SO4溶液,至恰好完全反应.产生气体的质量与所滴入H2SO4溶液的质量关系曲线如图所示.
在一烧杯中盛20g Na2CO3和Na2SO4的白色固体混合物,向其中逐滴滴加溶质质量分数为10%的H2SO4溶液,至恰好完全反应.产生气体的质量与所滴入H2SO4溶液的质量关系曲线如图所示.