题目内容
20.如图为实验室里制取气体时常用的部分仪器.
(1)若要组装一套CO2的制取装置,除了选择B、C还要选择图中的A、D、F,发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,检验气体是否收集满的方法是将燃着的木条放在集气瓶瓶口,观察木条是否熄灭;
(2)选用H装置除去二氧化碳中的水蒸气,其中的X是浓硫酸;
(3)要制得4.4g CO2气体,至少需要溶质质量分数为14.6%的稀盐酸的质量为50g.
分析 (1)根据发生装置和收集装置用到的仪器和二氧化碳的验满方法考虑;
(2)根据浓硫酸的吸水性考虑;
(3)根据方程式的书写方法和基本计算分析本题.
解答 解:(1)用长颈漏斗需要选择双孔塞,需要反应容器试管,收集二氧化碳用向上排空气法收集,所以除了选择B、C还要选择图中的ADF;在实验室中,常用大理石或石灰石与稀盐酸反应来制取二氧化碳,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳验满方法:将燃着的木条放在集气瓶口,如果熄灭,说明已经满了;故填:A、D、F; CaCO3+2HCl=CaCl2+H2O+CO2↑;将燃着的木条放在集气瓶瓶口,观察木条是否熄灭.
(2)浓硫酸具有吸水性,所以除去二氧化碳中的水蒸气,其中的X是浓硫酸;故填:浓硫酸;
(3)解:设需要14.6%的稀盐酸的质量为x,则
CaCO3+2HCl═CaCl2+CO2↑+H2O
73 44
x×14.6% 4.4g
$\frac{73}{44}=\frac{x×14.6%}{4.4g}$
x=50g
故填:50.
点评 固液常温型装置可用试管、单孔橡皮塞装置或长颈漏斗和双孔塞装置,固体加热型装置需用到酒精灯,气体的收集方法根据其密度和水溶性判断.

练习册系列答案
相关题目
10.甲和乙在一定条件下反应生成丙和丁,结合微观示意图分析,下列结论正确的是( )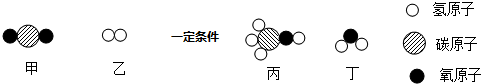

| A. | 该反应是置换反应 | |
| B. | 反应前后分子总数不变 | |
| C. | 发生反应的甲和乙的质量比为22:3 | |
| D. | 反应前后各元素的化合价不发生变化 |
5.最近科学家成功制备出了一种含铱(Ir)和氧两种元素的阳离子,在这种离子中铱元素显+9价,该离子的符号是( )
| A. | IrO4+ | B. | IrO5+ | C. | IrO3+ | D. | IrO2+ |
12.如图所示图象能正确反映其对应的实验操作的是( )
| A. | 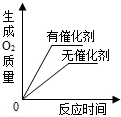 用等量、等浓度的双氧水制氧气 | |
| B. | 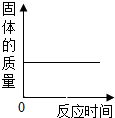 将向一定量的二氧化锰中加入过氧化氢溶液 | |
| C. | 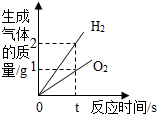 将水通电一段时间 | |
| D. | 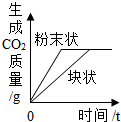 等质量CaCO3分别与等体积等浓度的稀盐酸(足量)反应 |
2.请设计一个实验,探究石蜡中是否含有碳元素和氢元素.
①问题:石蜡中含有哪些元素?
②猜想:石蜡中含有碳元素和氢元素
③实验验证
④结论:石蜡中含有碳元素和氢元素
⑤思考:你认为你所设计的实验能否证明石蜡中有没有氧元素,为什么?
①问题:石蜡中含有哪些元素?
②猜想:石蜡中含有碳元素和氢元素
③实验验证
| 实验操作 | 现象 | 分析 |
| 1 | ||
| 2 |
⑤思考:你认为你所设计的实验能否证明石蜡中有没有氧元素,为什么?

