题目内容
某同学将10g Na2CO3和NaOH的固体混合物投入到100g 7.3%的盐酸中,恰好完全反应,则原固体混合物钠元素的质量分数为( )
| A、40% | B、56% |
| C、46% | D、2 3% |
考点:根据化学反应方程式的计算,化合物中某元素的质量计算
专题:有关化学方程式的计算
分析:根据化学反应遵循质量守恒定律,在化学反应前后元素种类和质量不变,计算出生成氯化钠中钠元素的质量也就是混合物中钠元素的质量来解答本题.
解答:解:设生成氯化钠的质量为x;
HCl→NaCl
36.5 58.5
100g×7.3% x
=
x=11.7g
钠元素的质量:11.7g×
×100%=4.6g;
原固体混合物钠元素的质量分数:
×100%=46%,
答案:C.
HCl→NaCl
36.5 58.5
100g×7.3% x
| 36.5 |
| 100g×7.3% |
| 58.5 |
| x |
x=11.7g
钠元素的质量:11.7g×
| 23 |
| 58.5 |
原固体混合物钠元素的质量分数:
| 4.6g |
| 10g |
答案:C.
点评:根据化学反应遵循质量守恒定律,在化学反应前后元素种类和质量不变,由题目中的信息,找出已知量和未知量,根据化学方程式,正确列出比例式,计算出所求质量.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
如图所示的实验操作正确的是( )
A、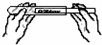 取用固体粉末 |
B、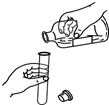 倾倒液体 |
C、 加热液体 |
D、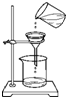 过滤 |
加碘盐中的碘元素以KIO3形式存在,其中碘元素的化合价是( )
| A、+7 | B、+5 | C、+3 | D、+1 |
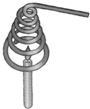 某同学在研究物质燃烧的条件时,做了如图所示的实验;把一条粗金属丝绕成线圈罩在一支蜡烛的火焰上,火焰很快就熄灭了.对这一实验的说法不正确的是( )
某同学在研究物质燃烧的条件时,做了如图所示的实验;把一条粗金属丝绕成线圈罩在一支蜡烛的火焰上,火焰很快就熄灭了.对这一实验的说法不正确的是( )| A、金属线圈内的气体温度升高 |
| B、可燃物的温度降到了着火点以下 |
| C、金属丝有良好的导热性 |
| D、若预先将金属丝加热,蜡烛就不会很快熄灭 |
下列化学用语书写不正确的是( )
| A、2个氧原子:O2 | ||||
B、2KClO3
| ||||
| C、氢氧根离子:OH- | ||||
| D、氧化铝Al2O3 |
 如图是甲、乙两种物质的溶解度曲线.t2℃时,在两个烧杯中分别加入甲、乙两种物质各Wg后,再分别加入100g水,充分搅拌.下列说法正确的是( )
如图是甲、乙两种物质的溶解度曲线.t2℃时,在两个烧杯中分别加入甲、乙两种物质各Wg后,再分别加入100g水,充分搅拌.下列说法正确的是( )| A、t2℃时,所得甲、乙两种物质的溶液均为饱和溶液 |
| B、甲物质的溶解度比乙物质的溶解度大 |
| C、温度降低到t1℃时,两杯溶液中溶质质量分数相等,得到甲、乙的不饱和溶液 |
| D、温度降低到t1℃时,甲物质的溶液中一定有固体析出 |
 多食油炸食物对健康不利,因为食物长时间煎炸后所产生的微量的丙烯醛等有毒物质会损害人体健康.丙烯醛的分子结构如图所示,下列说法正确的是( )
多食油炸食物对健康不利,因为食物长时间煎炸后所产生的微量的丙烯醛等有毒物质会损害人体健康.丙烯醛的分子结构如图所示,下列说法正确的是( )| A、丙烯醛分子由碳、氢、氧三种元素组成 |
| B、丙烯醛中碳、氧元素的质量比是3:1 |
| C、丙烯醛分子中含有三个碳原子 |
| D、丙烯醛的相对分子质量是56 |

