题目内容
16.钙是维持人体正常功能所必需的元素,有时需要服用补钙剂满足人体需求.如图分别为两种补钙剂说明书的一部分.
请根据图示中的信息回答下列问题:
(1)钙是人体必须的常量元素,每日要摄取足够量的钙,才能避免A(填字母序号);
A.佝偻病或骨质疏松症 B.贫血症 C.甲状腺肿大
(2)每片金钙尔奇中含碳酸钙的质量为700mg;
(3)按照金钙尔奇说明书每日的补钙量,若改用葡萄糖酸钙,一日3次,一次应服用几4片?
分析 (1)根据钙元素的生理功能来分析;
(2)根据一定质量的化合物中某元素的质量计算方法来分析;
(3)根据钙元素的质量相等来分析.
解答 解:(1)儿童缺钙易患佝偻病,成年人或老年人缺钙易患骨质疏松症;故填:A;
(2)碳酸钙(化学式为CaCO3)中钙元素的质量分数为:$\frac{40}{40+12+16×3}×100%$=40%;每片金钙尔奇中含碳酸钙的质量为:280mg÷40%=700mg;故填:700;
(3)每天服用的金钙尔奇中含钙元素的质量为280mg×2=560mg;每片葡萄糖酸钙片中,钙元素的质量为:0.5g×$\frac{40}{12×12+1×22+16×14+40}$×100%≈47mg.
则服用葡萄糖酸钙片,一日3次,每次:560mg÷47mg÷3≈4.
故填:4.
点评 本题主要考查学生运用化学式进行计算的能力,理解化学式的意义是解题的关键.

练习册系列答案
相关题目
7.如图所示的化学实验基本操作中,正确的是( )
| A. | 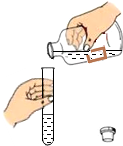 倾倒液体 | B. | 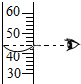 读取数值 | C. | 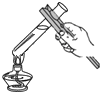 加热液体 | D. | 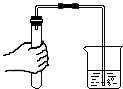 检查气密性 |
4. 用如图所示的装置进行电解水实验,有以下描述:
用如图所示的装置进行电解水实验,有以下描述:
①该实验可以证明水是由氢元素与氧元素组成的
②甲、乙两试管内收集到的气体的体积比约为2:1
③甲试管内产生的气体能燃烧
④甲、乙两试管内收集到的气体的质量比约为1:8
以上描述中正确的是( )
 用如图所示的装置进行电解水实验,有以下描述:
用如图所示的装置进行电解水实验,有以下描述:①该实验可以证明水是由氢元素与氧元素组成的
②甲、乙两试管内收集到的气体的体积比约为2:1
③甲试管内产生的气体能燃烧
④甲、乙两试管内收集到的气体的质量比约为1:8
以上描述中正确的是( )
| A. | ①②③④ | B. | ①③ | C. | ①② | D. | ①②③ |
11.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂.此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究.
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质是什么?
【进行猜想】①溶质可能只是CaCl2
②溶质可能是CaCl2与Ca(OH)2
③溶质可能是CaCl2与HCl
【实验探究】小明同学为了探究溶液中溶质的成分,进行了以下实验探究:
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁制下水道,可能造成的危害是腐蚀铁制下水道.要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量碳酸钙,充分反应后过滤.
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质是什么?
【进行猜想】①溶质可能只是CaCl2
②溶质可能是CaCl2与Ca(OH)2
③溶质可能是CaCl2与HCl
【实验探究】小明同学为了探究溶液中溶质的成分,进行了以下实验探究:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中,向试管中滴加几滴无色酚酞溶液,振荡 | 溶液不变色 | 猜想②不正确 |
| 猜想③正确 |
8.ClO2是新一代自来水消毒剂.如图为制取ClO2反应的微观示意图.下列有关该反应的说法正确的是( )
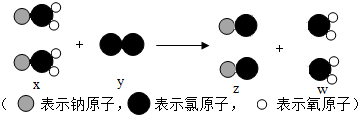

| A. | 该反应的化学方程式为:2NaClO2+Cl2═2NaCl+ClO2 | |
| B. | x是化合物,y单质 | |
| C. | z、w都是氧化物 | |
| D. | 该反应属于置换反应 |
6.测定生活中一些物质的pH,结果如图.下列说法错误的是( )


| A. | 食醋可以用于去除水垢 | |
| B. | 胃酸过多的人宜多喝柠檬汁 | |
| C. | 草木灰可改良酸性土壤 | |
| D. | 厨房清洁剂中含有氢氧化钠,可清洗炉具 |
