题目内容
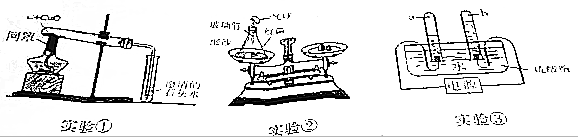
7.某化学兴趣小组设计了如图一套微型实验装置,用来测定一种石灰石样品中碳酸钙的质量数分数,具体做法是:
①从样品中取0.125g石灰石进行实验;
②加入稍过量的稀盐酸;
③实验后澄清石灰水质量增加0.044g(整过实验过程中称量、操作均正确,各反应均完全).计算:
(1)碳酸钙中①钙、碳元素的质量比为10:3;②氧元素的质量分数是48%.
(2)样品中碳酸钙质量分数的最大值是多少?
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%进行分析;
(2)根据二氧化碳的质量结合反应的化学方程式可以计算出样品中碳酸钙的质量,然后算出碳酸钙的质量分数即可.
解答 解:(1)碳酸钙中钙、碳元素的质量比为40:12=10:3,碳酸钙中氧元素的质量分数为:$\frac{16×3}{40+12+16×3}$×100%=48%;
(2)设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 0.044g
$\frac{100}{x}$=$\frac{44}{0.044g}$
x=0.1g
所以样品中碳酸钙质量分数的最大值是:$\frac{0.1g}{0.125g}$×100%=80%.
故答案为:(1)10:3,48%;
(2)80%.
点评 根据已知量计算方程式中其他物质的质量的计算方法,即可顺利解答,难度不大,要注意格式规范.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
18.某化合物隔绝空气加强热,生成二氧化碳和水,该化合物( )
| A. | 只含有碳和氢两种元素 | B. | 含有碳、氢、氧三种元素 | ||
| C. | 一定只含有碳、氢两种元素 | D. | 无法确定 |
4.某校“酸雨”测量小组的同学,取刚降落的雨水的水样,用pH探头(测pH的仪器)每隔几次测一次pH,其数据见表:
(1)根据所学知识,推测“正常雨水”的pH<7(填“<”“>”或“=”),引起这种pH的原因是空气中含有的二氧化碳能和水反应生成碳酸,碳酸显酸性.
(2)根据以上数据,判断所降雨水是否为“酸雨”?为什么?是,酸雨指的是pH小于5.6的雨水,观察表格提供的数据,雨水的pH都小于5.6,故是酸雨.
(3)经调查,这一地区有一个硫酸厂(生产过程中产生SO2)和一个电镀厂,这些厂使用的燃料主要是煤.试分析造成这一地区“酸雨”的主要原因是硫酸厂生产过程中产生的二氧化硫和煤燃烧产生的二氧化硫能和水反应生成显酸性的物质,从而形成酸雨.你认为可以采取哪些有效措施减少这一地区的“酸雨”?(至少答出两条)改用清洁燃料;产生的废气处理后再排放.
| 测定时间 | 3:10 | 3:15 | 3:20 | 3:25 | 3:30 | 3:35 | 3:40 |
| pH | 4.95 | 4.95 | 4.94 | 4.88 | 4.86 | 4.85 | 4.84 |
(2)根据以上数据,判断所降雨水是否为“酸雨”?为什么?是,酸雨指的是pH小于5.6的雨水,观察表格提供的数据,雨水的pH都小于5.6,故是酸雨.
(3)经调查,这一地区有一个硫酸厂(生产过程中产生SO2)和一个电镀厂,这些厂使用的燃料主要是煤.试分析造成这一地区“酸雨”的主要原因是硫酸厂生产过程中产生的二氧化硫和煤燃烧产生的二氧化硫能和水反应生成显酸性的物质,从而形成酸雨.你认为可以采取哪些有效措施减少这一地区的“酸雨”?(至少答出两条)改用清洁燃料;产生的废气处理后再排放.
5.小康同学的化学笔记中有以下知识总结,你认为正确的是( )
| A. | 碱性溶液不一定是碱溶液 | |
| B. | 稀溶液一定是不饱和溶液 | |
| C. | 固体物质的溶解度都随温度升高而增大 | |
| D. | 只由一种元素组成的物质都是单质 |