题目内容
8.下列有关物质除杂、检验、鉴别、分离的说法正确的是( )| A. | 向混有MgCl2的NaCl溶液中加入过量NaOH溶液,过滤得到无杂质的NaCl溶液 | |
| B. | 用水可以鉴别硫酸铜、氯化钠和碳酸钙三种固体物质 | |
| C. | 向某溶液中滴加稀盐酸,产生无色无味气体,则该溶液中一定含有碳酸氢根离子 | |
| D. | 依次通过溶解、过滤、蒸发三步操作,可分离硝酸钠和碳酸钾 |
分析 A、根据MgCl2能与过量NaOH溶液生成氢氧化镁沉淀和氯化钠,进行分析判断.
B、鉴别物质时,首先对需要鉴别的物质的性质进行对比分析找出特性,再根据性质的不同,选择适当的试剂,出现不同的现象的才能鉴别.
C、根据酸能与碳酸盐、碳酸氢盐溶液反应生成二氧化碳气体,进行分析判断.
D、根据硝酸钠和碳酸钾均易溶于水,进行分析判断.
解答 解:A、MgCl2能与过量NaOH溶液生成氢氧化镁沉淀和氯化钠,由于氢氧化钠溶液过量,过滤得到的是NaCl和氢氧化钠的混合溶液,故选项说法错误.
B、碳酸钙难难溶于水,硫酸铜、氯化钠分别溶于水形成蓝色溶液、无色溶液,可以鉴别,故选项说法正确.
C、向某溶液中滴加稀盐酸,产生无色无味气体,则该溶液中不一定含有碳酸氢根离子,也可能是含碳酸根离子,故选项说法错误.
D、硝酸钠和碳酸钾均易溶于水,不能用溶解、过滤、蒸发的方法进行分离,故选项说法错误.
故选:B.
点评 本题难度不大,掌握混合物分离的方法、物质鉴别题的原理、盐的化学性质等是正确解答本题的关键.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
18. 化学兴趣小组对“影响过氧化氢分解反应速率的因素--过氧化氢的质量分数和二氧化锰的用量”进行如下的实验探究,请你参与.
化学兴趣小组对“影响过氧化氢分解反应速率的因素--过氧化氢的质量分数和二氧化锰的用量”进行如下的实验探究,请你参与.
【进行实验】
在室温下,选用10mL不同溶质质量分数的过氧化氢溶液(5%和10%)分别与0.2g、0.8g和1.0g的二氧化锰粉末进行实验.
(1)过氧化氢分解反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
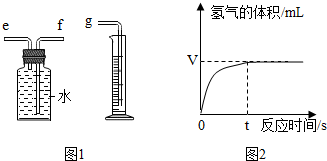
(2)用如图1所示装置收集并测量氧气的体积,其中量筒的作用是根据进入量筒中水的体积,判断生成氧气的体积,氧气应从e(选填e或f)管通入,再与g相连.
【数据处理】
(3)实验小组进行实验后,获得的相关实验数据如表所示:
①若要检验上述实验收集到的气体是否为氧气,方法是将带火星的木条伸入集气瓶中,若带火星的木条复燃,则证明是氧气.
②要比较不同质量分数的过氧化氢溶液对反应快慢的影响,应选择的实验编号是ad(写一组).由此可以得出的结论是:在催化剂、温度相同的条件下,过氧化氢的质量分数越大,反应速度越快.
③从上述实验中得出二氧化锰的用量对反应速率影响的结论是:在过氧化氢溶液的质量分数、温度相同的条件下,在一定的范围内,MnO2的用量越大,反应越快.
【拓展延伸】
(4)如图2是兴趣小组在记录生成氧气气体体积与对应时间的曲线,从曲线可以看出反应的速率逐渐变小,其原因是随着反应过氧化氢的质量分数变小,反应速度变慢.
(5)你认为影响过氧化氢分解反应速率的因素还有催化剂种类,请设计实验方案验证你的猜想取浓度相同、质量相同的过氧化氢溶液分别加入不同种类的同质量的催化剂进行实验,测定收集150mL氧气所需的时间即可.
 化学兴趣小组对“影响过氧化氢分解反应速率的因素--过氧化氢的质量分数和二氧化锰的用量”进行如下的实验探究,请你参与.
化学兴趣小组对“影响过氧化氢分解反应速率的因素--过氧化氢的质量分数和二氧化锰的用量”进行如下的实验探究,请你参与.【进行实验】
在室温下,选用10mL不同溶质质量分数的过氧化氢溶液(5%和10%)分别与0.2g、0.8g和1.0g的二氧化锰粉末进行实验.
(1)过氧化氢分解反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)用如图1所示装置收集并测量氧气的体积,其中量筒的作用是根据进入量筒中水的体积,判断生成氧气的体积,氧气应从e(选填e或f)管通入,再与g相连.
【数据处理】
(3)实验小组进行实验后,获得的相关实验数据如表所示:
| 实验编号 | 过氧化氢的质量分数 (均取10mL) | 二氧化锰粉末 的质量 | 氧气的体积(mL) (均收集5秒钟) |
| a | 5% | 0.2g | 65.8 |
| b | 5% | 0.8g | 85.7 |
| c | 5% | 1.0g | 85.7 |
| d | 10% | 0.2g | 121.9 |
| e | 10% | 0.8g | 171.5 |
| f | 10% | 1.0g | 171.5 |
②要比较不同质量分数的过氧化氢溶液对反应快慢的影响,应选择的实验编号是ad(写一组).由此可以得出的结论是:在催化剂、温度相同的条件下,过氧化氢的质量分数越大,反应速度越快.
③从上述实验中得出二氧化锰的用量对反应速率影响的结论是:在过氧化氢溶液的质量分数、温度相同的条件下,在一定的范围内,MnO2的用量越大,反应越快.
【拓展延伸】
(4)如图2是兴趣小组在记录生成氧气气体体积与对应时间的曲线,从曲线可以看出反应的速率逐渐变小,其原因是随着反应过氧化氢的质量分数变小,反应速度变慢.
(5)你认为影响过氧化氢分解反应速率的因素还有催化剂种类,请设计实验方案验证你的猜想取浓度相同、质量相同的过氧化氢溶液分别加入不同种类的同质量的催化剂进行实验,测定收集150mL氧气所需的时间即可.
19.某工厂排放的废气中含有NO、NO2、N2中的两种或三种,则该废气中氧元素的质量分数不可能是( )
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
3.金属是我们日常生活中接触较多的一种材料,下列说法正确的是( )
| A. | 黄铜(Cu-Zn合金)的硬度比铜的硬度小 | |
| B. | 铁生锈后生成的铁锈能阻止铁继续被锈蚀 | |
| C. | 将铁、铜与一定量的稀硫酸充分反应后,过滤,滤渣中一定只含铜 | |
| D. | 4Na+TiCl4(熔融)$\frac{\underline{\;高温\;}}{\;}$4NaCl+Ti,属于置换反应 |
20.下列物质属于纯净物的是( )
| A. | 紫菜蛋汤 | B. | 海水 | C. | 干冰 | D. | 新鲜空气 |
 A-F是初中化学常见的化合物,其转化关系如图所示,其中A,B,C都是氧化物,B能使澄清石灰水变浑浊,F是一种不溶于水的蓝色固体,图中“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).请回答:
A-F是初中化学常见的化合物,其转化关系如图所示,其中A,B,C都是氧化物,B能使澄清石灰水变浑浊,F是一种不溶于水的蓝色固体,图中“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).请回答: