题目内容
3.金属是我们日常生活中接触较多的一种材料,下列说法正确的是( )| A. | 黄铜(Cu-Zn合金)的硬度比铜的硬度小 | |
| B. | 铁生锈后生成的铁锈能阻止铁继续被锈蚀 | |
| C. | 将铁、铜与一定量的稀硫酸充分反应后,过滤,滤渣中一定只含铜 | |
| D. | 4Na+TiCl4(熔融)$\frac{\underline{\;高温\;}}{\;}$4NaCl+Ti,属于置换反应 |
分析 A、根据合金的硬度大于纯金属进行分析;
B、铁锈很疏松,不能阻碍里层的铁继续与氧气、水蒸气等反应;
C、根据金属与酸的反应进行分析;
D、根据置换反应的定义进行分析.
解答 解:A、黄铜是铜的合金,硬度大于纯铜,故错误;
B、铁锈很疏松,不能阻碍里层的铁继续与氧气、水蒸气等反应,铁制品表面的锈如不及时除去,会加快铁制品的生锈速度,故选项说法错误;
C、将铁、铜与一定量的稀硫酸充分反应,铜不与稀硫酸反应,滤渣中一定含有铜,没有说明铁是否全部反应,铁可能有剩余,所以滤渣中可能含有铁,故错误;
D、由反应方程式可知,该反应是单质和化合物反应生成单质和化合物,则属于置换反应,故正确;
故选D.
点评 本题主要考查了金属的性质,铁的锈蚀以及置换反应,难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
13.在实验复习课上,某合作学习小组的同学用碳酸钠溶液鉴别失去标签的稀硫酸、氢氧化钠溶液和氯化钡溶液.请你参与探究并填空:
【进行实验】
上述实验结束后,该组同学将A、B、C三支试管中的废液倒入同一烧杯中,然后过滤得到滤液①.为确定滤液①的成分,同学们进一步做了如下实验探究:
【实验结论】(4)同学们通过分析推理,得出结论:滤液①中共含有4种溶质.
【实验反思】(5)向滤液①中加入足量的氯化钡溶液的目的是除净滤液中①的Na2CO3,防止对下一步结果产生影响.
【进行实验】
| 实验操作 | 实验现象 | 实验结论 | |
| (1) | 分别用A、B、C三支试管取三种溶液各少量,然后再各加入一定量的碳酸钠溶液 | A中出现白色沉淀 B中有气泡生成 C中无明显现象 | A中的原溶液是氯化钡溶液 B中的原溶液是稀硫酸 C中的原溶液是氢氧化钠溶液 |
| 实验操作 | 实验现象 | 实验分析 | |
| (2) | 取少量滤液①于试管中,向其中加入足量的氯化钡溶液;过滤,得沉淀和滤液②,向沉淀中加入足量稀硝酸 | 产生白色沉淀 白色沉淀部分消失 | 根据实验现象可知,滤液①中含有 Na2CO3 、Na2SO4(填写溶质的化学式) |
| (3) | 取少量滤液②于试管中, 滴入足量酚酞 | 溶液变红 | 根据实验现象可知,滤液②中含有氢氧化钠 |
【实验反思】(5)向滤液①中加入足量的氯化钡溶液的目的是除净滤液中①的Na2CO3,防止对下一步结果产生影响.
11.下列操作中正确的是( )
| A. | 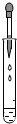 滴加液体 | B. | 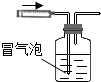 检查装置气密性 | ||
| C. | 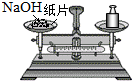 称量氢氧化钠固体 | D. | 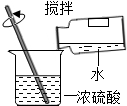 稀释浓硫酸 |
18.关于“舌尖上的化学”,下列说法不科学的是( )
| A. | 用甲醛溶液浸泡海产品,以延长保质期 | |
| B. | 为预防缺碘性疾病,可食用适量海带 | |
| C. | 食用“加铁酱油”,可补充铁元素,预防缺铁性贫血 | |
| D. | 为使发面食品松软可口,制作时可添加适量碳酸氢钠 |
8.下列有关物质除杂、检验、鉴别、分离的说法正确的是( )
| A. | 向混有MgCl2的NaCl溶液中加入过量NaOH溶液,过滤得到无杂质的NaCl溶液 | |
| B. | 用水可以鉴别硫酸铜、氯化钠和碳酸钙三种固体物质 | |
| C. | 向某溶液中滴加稀盐酸,产生无色无味气体,则该溶液中一定含有碳酸氢根离子 | |
| D. | 依次通过溶解、过滤、蒸发三步操作,可分离硝酸钠和碳酸钾 |
12.下列物质鉴别的方法中,不能区分开来的是( )
| A. | 用燃着的木条区分二氧化碳和氮气 | |
| B. | 用洁净的铁丝区分稀硫酸和氢氧化钠溶液 | |
| C. | 用观察法辨认氯酸钾和高锰酸钾固体 | |
| D. | 用盐酸区分氯化钠溶液和硝酸银溶液 |
13.下列实验操作错误的是( )
| A. | 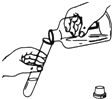 倾倒液体 | B. | 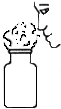 闻气体气味 | C. |  读液体体积 | D. |  稀释浓硫酸 |
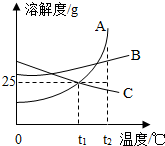 图中A、B、C分别表示三种不同的固体物质,其溶解度曲线如图所示.请回答下列问题:
图中A、B、C分别表示三种不同的固体物质,其溶解度曲线如图所示.请回答下列问题: 小江用无水醋酸钠和碱石灰固体混合加热制取甲烷,发生装置应该选择图中的装置A(选填“A”、“B”或“C”),如果用装置C来收集二氧化碳气体,则气体应该从m通入.
小江用无水醋酸钠和碱石灰固体混合加热制取甲烷,发生装置应该选择图中的装置A(选填“A”、“B”或“C”),如果用装置C来收集二氧化碳气体,则气体应该从m通入.