题目内容
11.应用常见金属在溶液中的活动性顺序能帮助我们进一步学习金属性质.分析下列反应,回答问题.A.Fe+CuSO4═FeSO4+Cu
B.Mg+MnSO4═Mn+MgSO4
C.Mn+FeSO4═Fe+MnSO4
(1)由此可以知道铁桶不能(选填“能”或“不能”)用来盛装CuSO4溶液;
(2)Fe、Cu、Mg、Mn四种金属的活动性由强到弱的顺序是Mg>Mn>Fe>Cu;
(3)Mn能否与稀硫酸反应?如果能,写出反应方程式,如果不能,说明理由Mn+H2SO4═MnSO4+H2↑.
分析 (1)根据金属活动性顺序表的应用分析回答;
(2)根据金属与酸、盐的反应情况分析金属的活动性由强到弱的顺序;
(3)根据Mn的活动性顺序分析.
解答 解:(1)由于铁能与硫酸铜反应,所以铁桶不能用来盛装CuSO4溶液;
(2)由Fe+CuSO4═FeSO4+Cu可知,铁的活动性大于铜;由Mg+MnSO4═Mn+MgSO4可知,镁的活动性大于锰;由Mn+FeSO4═Fe+MnSO4可知,锰的活动性大于铁;综合以上分析可知,Fe、Cu、Mg、Mn四种金属的活动性由强到弱的顺序是:Mg>Mn>Fe>Cu;
(3)由以上分析可知,锰的活动性大于铁,铁能与稀硫酸反应,Mn也能与稀硫酸反应,反应方程式为:Mn+H2SO4═MnSO4+H2↑.
故答为:(1)不能;(2)Mg>Mn>Fe>Cu;(3)Mn+H2SO4═MnSO4+H2↑.
点评 要熟练掌握氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
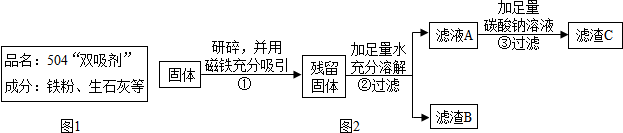
8.红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图1所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】甲同学的方案:
乙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁与稀盐酸反应生成的氯化铁又与铁粉反应生成氯化亚铁.
他设计如图2实验方案继续验证.
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使得铁粉能够充分吸引;
(2)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.
(3)③中反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
乙同学对滤渣B又进行探究.
【反思与评价】甲、乙两同学经过讨论后,完善实验方案最终确定该久置固体的成分是Fe、Fe2O3、CaO、CaCO3.

【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
取少量固体于试管中,滴 加足量的稀盐酸. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe, 一定不含Fe2O3. |
他设计如图2实验方案继续验证.
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使得铁粉能够充分吸引;
(2)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.
(3)③中反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
乙同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡产生、 澄清石灰水变浑浊、 溶液呈黄色. | 固体中一定含有CaCO3和Fe2O3. |
9.关于水的净化过程描述错误的是( )
| A. | 通过过滤装置除去可溶性杂质 | B. | 通入氯气杀菌消毒 | ||
| C. | 加入明矾使不溶性悬浮物凝聚 | D. | 通过活性炭吸附部分有害物质 |
6.下列各组物质在溶液中能大量共存且形成无色溶液的是( )
| A. | K2CO3 NaCl HCl | B. | CuSO4 H2SO4 NaNO3 | ||
| C. | BaCl2 AgNO3 Na2SO4 | D. | AlCl3 KNO3 Na2SO4 |
16.短周期(前三周期)元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的3倍,Y原子最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列说法正确的是( )
| A. | X元素可以与W元素形成XW2和XW3两种化合物 | |
| B. | Y元素的单质一定条件下可以与O2、N2、CO2反应 | |
| C. | Z原子的最外层电子数为4,形成化合物时一般为+4价 | |
| D. | X与Y、Z与W都属于同一周期 |
3.现有50克浓度为10%的KNO3溶液,要使其浓度增大一倍,可以采用的方法是( )
| A. | 蒸发掉25克水 | B. | 加水溶液变100克 | C. | 增加10克溶质 | D. | 增加6.25克溶质 |
20.如表是某同学设计的物质鉴别方法,他设计的两种方法都正确的是( )
| 选项 | 需鉴别的物质 | 加试剂或方法 | |
| 方法1 | 方法2 | ||
| A | 稀盐酸、氯化钾溶液 | 无色酚酞、看颜色 | 加入铁粉、看气泡 |
| B | 生石灰、熟石灰 | 两种物质分别溶于水 | 向两种物质中分别加入稀盐酸 |
| C | 蒸馏水、酒精 | 分别点燃 | 品尝 |
| D | 厕所清洁剂、厨房洗涤剂 | 用pH试纸测定它们的pH | 分别加入少量石蕊试液 |
| A. | A | B. | B | C. | C | D. | D |