题目内容
19.根据下列装置图,回答有关问题:
(1)图中标号仪器的名称:①酒精灯.
(2)利用上图中A、D装置的组合可以制取某种气体,实验室制取该气体的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室通常利用如图中装置B(选填字母)与D的组合制取二氧化碳,该反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.若用C装置代替B装置进行实验,优点为可以控制反应的发生和停止.
分析 酒精灯是常用的加热仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;C装置的优点是:可以控制反应的发生和停止.
解答 解:(1)酒精灯是常用的加热仪器,故答案为:酒精灯;
(2)如果用高锰酸钾制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;C装置的优点是:可以控制反应的发生和停止;故答案为:B;CaCO3+2HCl=CaCl2+H2O+CO2↑;可以控制反应的发生和停止;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.一种硫元素的氧化物中,硫元素和氧元素的质量比为2:3,则此硫原子和氧原子的个数比( )
| A. | 1:1 | B. | 1:3 | C. | 1:2 | D. | 3:1 |
8.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,其充分反应,实验数据如表:
(1)x的值为.
(2)黄铜样品中锌的质量分数为多少?
(3)所用稀硫酸的质量分数为多少?
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | x | 7.4 | 6.75 | 6.75 |
(2)黄铜样品中锌的质量分数为多少?
(3)所用稀硫酸的质量分数为多少?
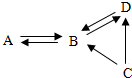 A、B、C、D均含有同一种元素,它们的转化关系如图(部分物质和反应条件已略去):
A、B、C、D均含有同一种元素,它们的转化关系如图(部分物质和反应条件已略去):

 结合在实验室里配制200g溶质质量分数为10%的NaOH溶液的实验,回答有关问题:
结合在实验室里配制200g溶质质量分数为10%的NaOH溶液的实验,回答有关问题: