题目内容
14.(1)利用如图1所示装置可测定空气中氧气的含量.
①实验现象,红色物质逐渐变成黑色.
②反应的化学方程式为2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO
③给足量的铜加热反应,充分反应后停止加热冷却至室温,注射器内气体的体积大约减少了约$\frac{1}{5}$.
④实验结论空气中氧气的体积分数大约为$\frac{1}{5}$.
(2)甲同学用如图2所示“测定空气中氧气的含量”,用碳代替红磷,结果发现集气瓶内并没有进入水,其原因是碳燃烧生成物是二氧化碳气体,瓶内气压不变; 而乙同学提出:将集气瓶中的水换成氢氧化钠溶液就能达到预期的结果.
分析 (1)在加热的条件下,铜丝与空气中的氧气反应生成黑色的氧化铜,停止加热冷却至室温,注射器内气体的体积大约减少了$\frac{1}{5}$,由此可以得出:空气中氧气的体积分数大约为$\frac{1}{5}$;
(2)根据碳燃烧生成物是二氧化碳气体,瓶内气压不变解答.
解答 解:
(1)在加热的条件下,铜丝与空气中的氧气反应生成黑色的氧化铜,反应的化学方程式为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;停止加热冷却至室温,注射器内气体的体积大约减少了$\frac{1}{5}$,由此可以得出:空气中氧气的体积分数大约为$\frac{1}{5}$;
(2)测空气中氧气的含量主要是根据物质燃烧消耗空气中的气体造成气压减小,减小的体积就是氧气的体积,故生成物中不能有气体,用碳代替红磷,碳燃烧生成物是二氧化碳气体,瓶内气压不变,故不会进入水;
乙同学要想得到正确的实验结论必须消耗掉生成的二氧化碳气体,故可选择氢氧化钠溶液吸收二氧化碳;
故答案为:
(1)①红色物质逐渐变成黑色 ②2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO ③约$\frac{1}{5}$ ④空气中氧气的体积分数大约为$\frac{1}{5}$;
(2)碳燃烧生成物是二氧化碳气体,瓶内气压不变;氢氧化钠.
点评 本题主要考查了用铜丝测定空气里氧气含量的实验原理、操作步骤、实验现象、反应的化学方程式、实验结论等.由于装有铜丝的玻璃管和注射器的前端较细,为了使注射器里的空气中的氧气能充分的与铜丝反应,在试验过程中应来回交替推动注射器的活塞.

练习册系列答案
相关题目
5.中国的金刚石探明储量和产量均居世界第10名左右,年产量在20万克拉,辽宁瓦房店是目前亚洲最大的金刚石矿山.下列有关金刚石的说法不正确的是( )
| A. | 金刚石是一种单质 | |
| B. | 金刚石、石墨都是由碳原子构成的 | |
| C. | 金刚石与石墨的物理性质不同是由于它们的结构不同 | |
| D. | 石墨与金刚石之间可以相互转化,它们之间的转化属于物理变化 |
2.正确的实验操作对实验结果、人身安全都非常重要.下列实验操作正确的是( )
| A. |  加热液体 | B. |  过滤 | C. |  稀释浓硫酸 | D. |  称量固体 |
9.下列反应属于分解反应的是( )
| A. | 硫在氧气中燃烧 | B. | 氯酸钾和二氧化锰混合加热制氧气 | ||
| C. | 铁在氧气中燃烧 | D. | 蜡烛燃烧 |
6.已知:饱和溶液,不饱和溶液,稀溶液,浓溶液之间的关系如图列说法不正确的是( )
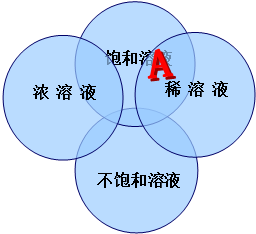

| A. | 图中A处的含义饱和的稀溶液 | |
| B. | 浓溶液一定是饱和溶液,稀溶液一定不饱和 | |
| C. | 在一定的温度下向饱和的硝酸钾溶液中加入少量的硝酸钾晶体,晶体不再溶解 | |
| D. | 同一温度下,同种溶质的饱和溶液一定比它的不饱和溶液浓 |
3.为研究锌和铝的金属活动性,某研究小组进行了如下探究.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出锌与盐酸反应的化学方程式:Zn+2HCl═ZnCl2+H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是未去膜的铝片表面有氧化铝(氧化膜),氧化铝先与盐酸反应.
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝(或铝和氯化铝的混合物);
假设b:该灰黑色沉淀可能含有AlCl3;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如下实验.
【得出结论】由实验①可判断假设c不成立(填“成立”或“不成立”),再集合②和③可得出该灰黑色沉淀的成分是铝和氯化铝.
(4)你认为①中小明的实验能否比较锌和铝的金属活动性强弱?不能(填“能”或“不能”),分别从设计方法和操作可行性的角度,具体说明理由:设计方法角度:小明的实验方案中未控制金属的纯度,盐酸的浓度等相关变量相同;
操作可行性角度:操作中难以做到铝片和锌粒的表面积相同..
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出锌与盐酸反应的化学方程式:Zn+2HCl═ZnCl2+H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是未去膜的铝片表面有氧化铝(氧化膜),氧化铝先与盐酸反应.
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝(或铝和氯化铝的混合物);
假设b:该灰黑色沉淀可能含有AlCl3;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如下实验.
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
(4)你认为①中小明的实验能否比较锌和铝的金属活动性强弱?不能(填“能”或“不能”),分别从设计方法和操作可行性的角度,具体说明理由:设计方法角度:小明的实验方案中未控制金属的纯度,盐酸的浓度等相关变量相同;
操作可行性角度:操作中难以做到铝片和锌粒的表面积相同..
 等质量的M、N两种金属,分别与相同质量分数、等质量的稀盐酸反应成生氢气质量和反应时间的关系如图所示.
等质量的M、N两种金属,分别与相同质量分数、等质量的稀盐酸反应成生氢气质量和反应时间的关系如图所示.