题目内容
20.用如图提供的装置与试剂,组装一套用CO还原CuO的实验装置,并回答问题.(C内盛有还原CuO的CO)
(1)实验时气体按图示从左向右移动,则这套装置的连接顺序是(填接口处字母):e接b,c接a.
(2)实验开始时是先通一氧化碳,还是先加热氧化铜先通一氧化碳,这样做的原因是防止气体不纯,加热时发生爆炸;B中发生反应的化学方程式为CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)装置A中足量澄清石灰水的作用:检验二氧化碳.
(4)实验后怎样处理气球中的尾气点燃发生反应的化学方程式为2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
分析 (1)根据一氧化碳还原氧化铜的反应特点组装仪器;
(2)根据实验注意事项进行分析;根据反应物、生成物及质量守恒定律书写;
(3)根据题目信息可知,澄清石灰水是检验二氧化碳;
(4)尾气为一氧化碳,根据其具有可燃性进行分析;
解答 解:(1)根据一氧化碳还原氧化铜时,先通入一氧化碳、加热反应、检验生成物、尾气吸收,连接装置的顺序为:e接b,c接a;
(2)由于一氧化碳气体是可燃性气体,所以在点燃前要先通入一氧化碳气体使装置中的空气排净,然后再加热,防止气体不纯,加热时发生爆炸;B中发生反应的化学方程式为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(3)根据题目信息可知需要检验二氧化碳,检验二氧化碳常用澄清石灰水,反应现象是石灰水变浑浊;
(4)一氧化碳有毒性,所以要进行尾气处理,防止污染空气,反应后应将气体烧掉,反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
故答案为:
(1)e接b,c接a;(2)先通一氧化碳,防止气体不纯,加热时发生爆炸,CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)检验二氧化碳(4)点燃,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
点评 学会根据实验注意事项分析问题,同时记住一氧化碳的性质,以及化学方程式的正确书写,环保方法使用等.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目
11.配平下列化学方程式
①8NH3+6NO2=7N2+12H2O;
②16P+15H2O=10PH3+3P2O5;
③1C2H6O+3O2=2CO2+3H2O;
④1CH4+2O2=1CO2+2H2O.
①8NH3+6NO2=7N2+12H2O;
②16P+15H2O=10PH3+3P2O5;
③1C2H6O+3O2=2CO2+3H2O;
④1CH4+2O2=1CO2+2H2O.
12.做完“铁在氧气里燃烧”实验后,小明同学有两个疑惑不解的问题,于是他进行了以下探究活动,请你一同参与.
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液,但不产生氢气.
(3)颜色:Fe粉-黑色,FeO-黑色,Fe3O4-黑色,Fe2O3-红棕色
【实验探究】
将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是产生气泡,说明铁燃烧时溅落下来的黑色物质中还含有铁.
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
【查阅资料2】
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(2)Fe2O3高温时分解成Fe3O4.
【理论探讨】
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在1400℃~1538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须在集气瓶底部铺一层细沙,或加入适量的水;
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑;
(3)有些超市的食品密封包装盒的透明盖内放有FeO粉末,若粉末的颜色由黑色变成红棕色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液,但不产生氢气.
(3)颜色:Fe粉-黑色,FeO-黑色,Fe3O4-黑色,Fe2O3-红棕色
【实验探究】
将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是产生气泡,说明铁燃烧时溅落下来的黑色物质中还含有铁.
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(2)Fe2O3高温时分解成Fe3O4.
【理论探讨】
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在1400℃~1538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须在集气瓶底部铺一层细沙,或加入适量的水;
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑;
(3)有些超市的食品密封包装盒的透明盖内放有FeO粉末,若粉末的颜色由黑色变成红棕色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
1.如图所示实验装置进行的相应实验,达不到实验目的是( )


| A. | 在实验室中,用图1所示装置除去少量黄河水中的泥沙 | |
| B. | 用图2所示装置除去CO2中含有的少量HCl气体 | |
| C. | 用图3所示装置制取少量CO2气体 | |
| D. | 用图4所示装置稀释浓硫酸 |
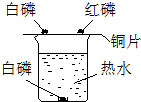 探究燃烧条件的实验装置如图所示.
探究燃烧条件的实验装置如图所示. 化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
 ,该元素在常温下与氧气反应的方程为2Al+3O2═2Al2O3
,该元素在常温下与氧气反应的方程为2Al+3O2═2Al2O3 ,而He的化学性质不活泼(填“活泼”或“不活泼”);由此可知,最外层电子数相同时,化学性质不一定(填“一定”或“不一定”)相似.
,而He的化学性质不活泼(填“活泼”或“不活泼”);由此可知,最外层电子数相同时,化学性质不一定(填“一定”或“不一定”)相似.
