题目内容
11.某化工厂排出的废液中含有AgNO3、Zn(NO3)2和Cu(NO3)2三种物质.为了分离并回收金属银和铜,化学课外小组的同学设计了如下实验方案: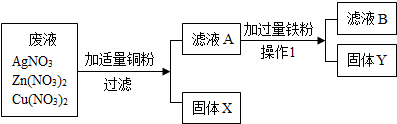
根据以上实验方案你认为:
固体X是银,得到固体X的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag;固体Y是铜和铁混合物,滤液B中的溶质是Zn(NO3)2、Fe(NO3)2,操作1名称是过滤.
分析 在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能把位于其后的金属从其盐溶液中置换出来.过滤能将固液分开.据此分析回答有关的问题.
解答 解:由实验的方案可知,要分离并回收金属银和铜,可以利用金属与盐溶液的反应来进行,加入适量铜粉,能把废液中硝酸银中的银置换出来,所以固体X是银,反应的化学方程式是:Cu+2AgNO3═Cu(NO3)2+2Ag;得到的滤液中含有硝酸锌和硝酸铜,加入过量的铁粉,能与滤液A中的硝酸铜反应生成铜和硝酸亚铁,由于铁过量,反应后有剩余,故所得固体Y中含有铜和铁,滤液B中含有硝酸亚铁和硝酸锌.操作1能将固体和也分开名称是过滤.
故答案为:银;Cu+2AgNO3═Cu(NO3)2+2Ag; 铁和铜的混合物; Zn(NO3)2、Fe(NO3)2; 过滤.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
1.下列变化属于化学变化的是( )
| A. | 干冰升华 | B. | 海水晒盐 | C. | 浓硫酸吸水 | D. | 瓦斯爆炸 |
6.下列用途利用其化学性质的是( )
| A. | 食品包装时充入氮气 | B. | 干冰用于人工降雨 | ||
| C. | 用铜作为导线 | D. | 用石墨做铅笔芯 |
16.在配制10%氯化钠溶液的过程中,会导致溶液中氯化钠的质量分数大于10%的原因可能是( )
| A. | 盛装溶液的试剂瓶中有少量10%的氯化钠溶液 | |
| B. | 称量氯化钠固体时所用天平的砝码缺了一个角 | |
| C. | 用量筒量取水时俯视读数 | |
| D. | 将称量好的氯化钠固体倒入烧杯中时,有部分氯化钠固体散落在实验桌上 |
 A、B、C、D是初中常见的物质,A是由核电荷数分别为6、8、11的三种元素组成的化合物,B是一种微溶性碱,C是一种可溶性盐酸盐,D是一种可溶性碱,它们之间存在的关系如图所示,图中“-”表示物质间能发生的化学反应,“→”表示物质间的转化关系.
A、B、C、D是初中常见的物质,A是由核电荷数分别为6、8、11的三种元素组成的化合物,B是一种微溶性碱,C是一种可溶性盐酸盐,D是一种可溶性碱,它们之间存在的关系如图所示,图中“-”表示物质间能发生的化学反应,“→”表示物质间的转化关系.

