题目内容
16.小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应).操作过程如下:请计算:
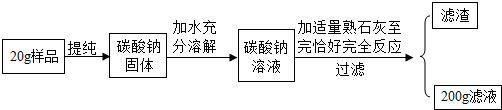
(1)20g样品中碳酸钠的质量为10.6g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200g滤液浓缩成制作“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水120g.
分析 (1)碳酸钠的质量=样品的质量×含碳酸钠的质量分数;
(2)根据化学方程式结合碳酸钠的质量求解氢氧化钠的质量,进一步计算所得滤液中氢氧化钠的质量分数.
(3)根据溶液稀释前后溶质质量不变解答.
解答 解:(1)碳酸钠的质量为20g×53%=10.6g;
(2)设反应生成氢氧化钠的质量为x;
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
10.6g x
$\frac{106}{10.6g}=\frac{80}{x}$
解得x=8g
氢氧化钠的质量分数=$\frac{8g}{200g}$×100%=4%
答:反应后所得滤液中氢氧化钠的质量分数为4%.
(3)设需蒸发水y
200g×4%=(200g-y)×10%
y=120g
故答案为:
(1)10.6;
(2)4%;
(3)120.
点评 本题重点考查了化学方程式的有关计算方法、步骤和格式;它是一道很传统的根据化学方程式计算的题目.解答时,只要细心地分析审题后,按照有关化学方程式的计算步骤和格式,进行计算即可.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
6.水中好坏直接影响人的健康,高铁酸钾(K2FeO4)是一种新型高效净水处理剂.高铁酸钾是暗紫色粉末,溶于水中生成紫红色溶液.下列有关高铁酸钾的分析中,正确的是( )
| A. | 高铁酸钾是一种氧化物 | B. | 高铁酸钾中铁元素的化合价是+3价 | ||
| C. | 高铁酸钾是由三种元素组成 | D. | 高铁酸钾中含有单质铁 |
7.在装有水的烧杯中分别加入以下物质,其中形成的溶液温度降低的是( )
| A. | 生石灰 | B. | 氢氧化钠 | C. | 氯化钠 | D. | 硝酸铵 |
4.下列物质不属于空气污染物的是( )
| A. | 二氧化硫 | B. | 一氧化碳 | C. | 氮气 | D. | 可吸入颗粒物 |
1.焰色反应火焰呈黄色的物质是( )
| A. | KCl | B. | NaCl | C. | CaCl2 | D. | CuCl2 |
8.化学反应C+H2O$\stackrel{高温}{→}$H2+CO中的还原剂是( )
| A. | C | B. | H2O | C. | H2 | D. | CO |
5.下列说法正确的是( )
| A. | 凡是均一的、稳定的液体一定是溶液 | |
| B. | 洗涤剂能够洗涤油污是因为洗涤剂能够溶解油污 | |
| C. | 饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液 | |
| D. | 5g某物质完全溶于水配成100g溶液,所得溶液的溶质质量分数一定是5% |
6.某化学反应可表示为:二氧化碳+水→M+氧气,根据以上信息,下列关于M组成的说法中正确的是( )
| A. | 一定含有C、H元素,可能含有O元素 | B. | 只含有C、H元素 | ||
| C. | 含有C、H、O三种元素 | D. | 无法确定 |