题目内容
化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题:

(1)写出图中带有标号仪器的名称:a ,b .
(2)实验室制取氧气、氢气、二氧化碳气体时,选用A、E装置可制取并收集 ;选用B、E装置可制取并收集 ;制取并收集二氧化碳气体应选用的装置是 ,选用的理由是 .
(3)实验室用A和C装置可制取氧气,请写出氯酸钾与二氧化锰混合加热制氧气的化学方程式 .其中二氧化锰的作用是 .
(4)实验室用高锰酸钾制氧气并用排水法收集,实验时应在试管口放 ,收集氧气的合适时机是 .
(5)现要制取1.6克氧气,需要高锰酸钾的质量是多少?

(1)写出图中带有标号仪器的名称:a
(2)实验室制取氧气、氢气、二氧化碳气体时,选用A、E装置可制取并收集
(3)实验室用A和C装置可制取氧气,请写出氯酸钾与二氧化锰混合加热制氧气的化学方程式
(4)实验室用高锰酸钾制氧气并用排水法收集,实验时应在试管口放
(5)现要制取1.6克氧气,需要高锰酸钾的质量是多少?
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,制取氧气的操作步骤和注意点,催化剂的特点与催化作用,根据化学反应方程式的计算
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)据常用仪器回答;
(2)A装置适用于加热固体制取气体,E装置收集不溶于水的气体,实验室可用加热氯酸钾或高锰酸钾的方法制取氧气,且氧气不易溶于水,所以可用AE装置制取氧气;B装置适用于固体和液体不需加热 制取气体,因此BE装置可用于锌和稀硫酸反应制取氢气,因为氢气不溶于水,二氧化碳能溶于水;实验室制取二氧化碳用大理石和稀盐酸常温反应,二氧化碳密度比空气大且能溶于水,据此选择发生和收集装置;
(3)据加热氯酸钾的反应原理书写方程式,二氧化锰在该反应中加速化学反应速率,而本身的质量和化学性质不变,起催化剂的作用;
(4)若用高锰酸钾制取,须在试管口放一些棉花,防止加热时高锰酸钾粉末进入导管;利用排水法收集时要等导管口气泡连续、均匀冒出再收集,防止收集的气体不纯;
(5)据加热高锰酸钾分解的方程式和氧气的质量计算需要高锰酸钾的质量.
(2)A装置适用于加热固体制取气体,E装置收集不溶于水的气体,实验室可用加热氯酸钾或高锰酸钾的方法制取氧气,且氧气不易溶于水,所以可用AE装置制取氧气;B装置适用于固体和液体不需加热 制取气体,因此BE装置可用于锌和稀硫酸反应制取氢气,因为氢气不溶于水,二氧化碳能溶于水;实验室制取二氧化碳用大理石和稀盐酸常温反应,二氧化碳密度比空气大且能溶于水,据此选择发生和收集装置;
(3)据加热氯酸钾的反应原理书写方程式,二氧化锰在该反应中加速化学反应速率,而本身的质量和化学性质不变,起催化剂的作用;
(4)若用高锰酸钾制取,须在试管口放一些棉花,防止加热时高锰酸钾粉末进入导管;利用排水法收集时要等导管口气泡连续、均匀冒出再收集,防止收集的气体不纯;
(5)据加热高锰酸钾分解的方程式和氧气的质量计算需要高锰酸钾的质量.
解答:解:(1)标号仪器分别是:酒精灯、长颈漏斗;
(2)A装置适用于加热固体制取气体,E装置收集不溶于水的气体,实验室可用加热氯酸钾或高锰酸钾的方法制取氧气,且氧气不易溶于水,所以可用AE装置制取氧气;B装置适用于固体和液体不需加热 制取气体,因此BE装置可用于锌和稀硫酸反应制取氢气,因为氢气不溶于水,二氧化碳能溶于水;实验室制取二氧化碳用大理石和稀盐酸常温反应,故选发生装置B,二氧化碳密度比空气大且能溶于水,故用向上排空气法收集;
(3)加热氯酸钾、二氧化锰作催化剂,生成氯化钾和氧气,反应的方程式是:2KClO3
2KCl+3O2↑;二氧化锰在该反应中加速化学反应速率,而本身的质量和化学性质不变,起催化剂的作用;
(4)若用高锰酸钾制取,须在试管口放一些棉花,防止加热时高锰酸钾粉末进入导管;利用排水法收集时要等导管口气泡连续、均匀冒出再收集,防止收集的气体不纯;
(5)设需要高锰酸钾的质量是x
2KMnO4
K2MnO4+MnO2+O2↑
316 32
x 1.6g
=
x=15.8g
故答案为:(1)酒精灯;长颈漏斗;
(2)氧气;氢气;BC;反应物是固体和液体,且不需加热;
(3)2KClO3
2KCl+3O2↑;催化作用;
(4)一团棉花;导管口气泡连续、均匀冒出时;
(5)需要高锰酸钾的质量是15.8g.
(2)A装置适用于加热固体制取气体,E装置收集不溶于水的气体,实验室可用加热氯酸钾或高锰酸钾的方法制取氧气,且氧气不易溶于水,所以可用AE装置制取氧气;B装置适用于固体和液体不需加热 制取气体,因此BE装置可用于锌和稀硫酸反应制取氢气,因为氢气不溶于水,二氧化碳能溶于水;实验室制取二氧化碳用大理石和稀盐酸常温反应,故选发生装置B,二氧化碳密度比空气大且能溶于水,故用向上排空气法收集;
(3)加热氯酸钾、二氧化锰作催化剂,生成氯化钾和氧气,反应的方程式是:2KClO3
| ||
| △ |
(4)若用高锰酸钾制取,须在试管口放一些棉花,防止加热时高锰酸钾粉末进入导管;利用排水法收集时要等导管口气泡连续、均匀冒出再收集,防止收集的气体不纯;
(5)设需要高锰酸钾的质量是x
2KMnO4
| ||
316 32
x 1.6g
| 316 |
| x |
| 32 |
| 1.6g |
x=15.8g
故答案为:(1)酒精灯;长颈漏斗;
(2)氧气;氢气;BC;反应物是固体和液体,且不需加热;
(3)2KClO3
| ||
| △ |
(4)一团棉花;导管口气泡连续、均匀冒出时;
(5)需要高锰酸钾的质量是15.8g.
点评:了解并掌握实验室利用高锰酸钾制取氧气、氢气、二氧化碳的反应原理、实验注意事项、装置选取方法等知识,并能据题意灵活解答问题.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
 材料一:近期天凉,流感病人越来越多了,为了预防该病毒,我们可用84消毒液进行消毒.
材料一:近期天凉,流感病人越来越多了,为了预防该病毒,我们可用84消毒液进行消毒. 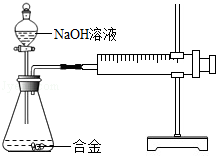 合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动. 如图,用红磷燃烧来测定空气中氧气的含量
如图,用红磷燃烧来测定空气中氧气的含量
