题目内容
2.下列变化中,属于化学变化的是( )| A. | 风力发电 | B. | 石油蒸馏 | C. | 净化水 | D. | 煤的干馏 |
分析 本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化.
解答 解:A、风力发电是利用轮子的转动发电,没有新物质生成,属于物理变化,故A错;
B、石油蒸馏是利用沸点不同,进行混合物的分离,属于物理变化,故B错;
C、净化水是将水中杂质除掉,没有新物质生成,属于物理变化,故C错;
D、煤的干馏生成煤焦油、焦炉气等新物质,属于化学变化,故D正确.
故选D.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
18.化学课上,同学们做了如下两个实验.
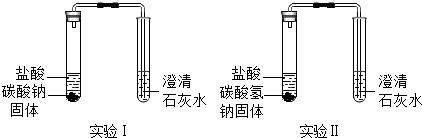
在实验过程中用手触摸试管,发现盛Na2CO3的试管变热,盛NaHCO3的试管变冷
【提出问题】两个实验过程中,温度变化的原因是什么?
【猜想与假设】甲同学认为:Na2CO3和盐酸反应为放热反应,而NaHCO3和盐酸反应为吸热反应.
乙同学认为甲的猜想有不足之处.
【设计实验】乙同学欲通过实验进行研究,实验步骤如下:
①分别向盛有0.5g Na2CO3固体、0.5g NaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度t1
②静置,测量温度t2
③分别加入10mL 密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度t3
【实验记录】多次实验后取平均值记录如下:
【分析与结论】
(1)甲同学猜想的不足之处是没有考虑固体溶解时的温度变化.通过步骤①得到的结论是Na2CO3固体溶解放热,NaHCO3固体溶解吸热.
(2)通过步骤②和③得到的结论是:Na2CO3和NaHCO3与盐酸反应都是放热反应.
【反思与评价】老师指出乙的设计仍存在不足,并补充做如下实验:向盛有10mL水(20℃)的烧杯中加入10mL密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度为22.2℃.
(1)此实验的目的是探究盐酸稀释过程中的温度变化.
(2)结合此次探究活动,你认为下列说法不正确的是B(填序号).
A.盐酸的稀释过程是放热过程
B.NaHCO3与盐酸的反应是放热反应
C.实验Ⅰ和Ⅱ中的能量变化与化学反应、物质的溶解和稀释有关.

| 实验装置 | 实验现象 | 实验结论 |
| | 实验Ⅰ、Ⅱ中均观察到:白色固体逐渐减少,有气泡冒出;澄清石灰水变浑浊. | Na2CO3和NaHCO3都能与盐酸反应产生CO2;NaHCO3与盐酸反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑. |
【提出问题】两个实验过程中,温度变化的原因是什么?
【猜想与假设】甲同学认为:Na2CO3和盐酸反应为放热反应,而NaHCO3和盐酸反应为吸热反应.
乙同学认为甲的猜想有不足之处.
【设计实验】乙同学欲通过实验进行研究,实验步骤如下:
①分别向盛有0.5g Na2CO3固体、0.5g NaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度t1
②静置,测量温度t2
③分别加入10mL 密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度t3
【实验记录】多次实验后取平均值记录如下:
| t1/℃ | t2/℃ | t3/℃ | |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
(1)甲同学猜想的不足之处是没有考虑固体溶解时的温度变化.通过步骤①得到的结论是Na2CO3固体溶解放热,NaHCO3固体溶解吸热.
(2)通过步骤②和③得到的结论是:Na2CO3和NaHCO3与盐酸反应都是放热反应.
【反思与评价】老师指出乙的设计仍存在不足,并补充做如下实验:向盛有10mL水(20℃)的烧杯中加入10mL密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度为22.2℃.
(1)此实验的目的是探究盐酸稀释过程中的温度变化.
(2)结合此次探究活动,你认为下列说法不正确的是B(填序号).
A.盐酸的稀释过程是放热过程
B.NaHCO3与盐酸的反应是放热反应
C.实验Ⅰ和Ⅱ中的能量变化与化学反应、物质的溶解和稀释有关.
10.工业上用电解饱和食盐水的方法来制取烧碱,将制得的烧碱溶液再经浓缩、蒸发等操作制成烧碱固体.在生产过程中,原料通常不能完全转化.另外,如果烧碱固体长时间存放在仓库里,也可能会变质.
(1)电解饱和食盐水制得烧碱的同时,还生成氯气和另一种气体,该反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
(2)现从仓库中取来烧碱样品,该样品除了可能含有纯碱杂质外,还可能含有氯化钠杂质.某化学小组决定探究样品中是否含有这两种杂质.
①查阅资料:实验中若产生微溶物质,通常会以沉淀形式存在.
②实验设计
③交流与反思
a.烧碱固体长时间在仓库存放会变质的原因是(用化学反应方程式表示)2NaOH+CO2=Na2CO3+H2O.
b.实验后若测得废液的pH<7,则废液呈酸性(填“酸性”、“中性”或“碱性”),从操作简单和经济环保的角度考虑,应向废液中加入稍过量的石灰石,然后再倒入下水道中.
(1)电解饱和食盐水制得烧碱的同时,还生成氯气和另一种气体,该反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
(2)现从仓库中取来烧碱样品,该样品除了可能含有纯碱杂质外,还可能含有氯化钠杂质.某化学小组决定探究样品中是否含有这两种杂质.
①查阅资料:实验中若产生微溶物质,通常会以沉淀形式存在.
②实验设计
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| a.取少量样品于试管中,并加入过量的稀硝酸. | 有气泡生成. | 样品中有纯碱. |
| b.再向步骤Ⅰ中所得的溶液加入硝酸银溶液. | 有白色沉淀生成. | 样品中有氯化钠. |
a.烧碱固体长时间在仓库存放会变质的原因是(用化学反应方程式表示)2NaOH+CO2=Na2CO3+H2O.
b.实验后若测得废液的pH<7,则废液呈酸性(填“酸性”、“中性”或“碱性”),从操作简单和经济环保的角度考虑,应向废液中加入稍过量的石灰石,然后再倒入下水道中.
7.下列应用和相应的原理(用化学方程式表示)及基本反应类型正确的是( )
| 选项 | 物质的应用 | 化学方程式 | 反应类型 |
| A | 电解水 | 2H202$\frac{\underline{\;通电\;}}{\;}$2H20+02↑ | 分解反应 |
| B | 向烧碱溶液中通人CO2 | 2NaOH+C02═Na2C03+H20 | 复分解反应 |
| C | 溶洞的形成 | CaC03+H20+C02═Ca(HC03)2 | 化合反应 |
| D | 比较铜和银的活动性 | Cu+AgN03═Cu(NO3)2+Ag | 置换反应 |
| A. | A | B. | B | C. | C | D. | D |
12. A、B、C三种物质的溶解度曲线如图所示.下列分析正确的是( )
A、B、C三种物质的溶解度曲线如图所示.下列分析正确的是( )
 A、B、C三种物质的溶解度曲线如图所示.下列分析正确的是( )
A、B、C三种物质的溶解度曲线如图所示.下列分析正确的是( )| A. | t1℃时两物质的饱和溶液中溶质的质量相等 | |
| B. | t2℃时将50g物质放入50g水中,得到A的饱和溶液,且其中溶质和溶剂质量比为1:1 | |
| C. | t1℃时三种物质的饱和溶液升高温度时,其溶质质量分数均保持不变 | |
| D. | 将t2℃时三种物质的饱和溶液恒温蒸发等量水分后,析出溶质的质量:A>B>>C |

 甲、乙两种固体的溶解度曲线如图所示.
甲、乙两种固体的溶解度曲线如图所示.