题目内容
9.在一密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表:| 物 质 | A | B | C | D |
| 反应前质量/g | 8 | 2 | 28 | 10 |
| 反应后质量/g | x | 2 | 3 | 21 |
(2)任写一例与上述反应类型相同的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 根据质量守恒定律进行分析,反应后质量增加的是生成物,减少的是反应物.由表格信息可知8g+2g+28+10g=x+2g+3g+21g,反应后x质量为22克,A质量增加是生成物;C质量减少了也是反应物;B质量不变,可能做催化剂,D质量增加的是生成物,符合“多一变多”的特点,是分解反应.
解答 解:根据质量守恒定律进行分析,反应后质量增加的是生成物,减少的是反应物.由表格信息可知8g+2g+28+10g=x+2g+3g+21g,反应后x质量为22克,A质量增加是生成物;C质量减少了也是反应物;B质量不变,可能做催化剂,D质量增加的是生成物,符合“多一变多”的特点,是分解反应.
(1)这一反应类型是分解反应;x=22g;由表中数据分析可知,B质量不变,可能没有参加反应,也可能是该反应的催化剂;
(2)写一个分解反应即可,如:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故答案为:(1)分解;22;催化剂;
(2)2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 解此题需根据质量守恒定律,认真分析各物质的质量变化情况,仔细推敲,即可求解.

练习册系列答案
相关题目
19.下列做法不正确的是( )
| A. | 电器失火后首先要切断电源 | |
| B. | 进入久未开启的地窖前先做灯火实验 | |
| C. | 厨房煤气泄漏后立即打开抽油烟机 | |
| D. | 燃放烟花爆竹时,远离人群和可燃物 |
20.下列做法正确的是( )
| A. | 电器着火时立即用水扑灭 | B. | 用肥皂水区分硬水和软水 | ||
| C. | 霉变的大米需要煮熟后食用 | D. | 在房间内放盆水可以防止煤气中毒 |
4. 小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应,老师告诉同学们,高温下,铁与水蒸气能反应生产一种常见的铁的氧化物和一种气体,小杰很好奇,设计如图实验探究铁粉与水蒸气反应后的产物.
小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应,老师告诉同学们,高温下,铁与水蒸气能反应生产一种常见的铁的氧化物和一种气体,小杰很好奇,设计如图实验探究铁粉与水蒸气反应后的产物.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是氢气.
(3)探究试管汇总剩余固体成分是什么?
【查阅资料】常见的铁的氧化物有FeO(黑色、没有磁性)、Fe2O3,Fe3O4
【初步验证】试管中固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe3O4,猜想二:剩余固体是Fe与Fe3O4
【实验探究】
【实验结论】铁和水蒸气反应的化学方程式:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2↑.
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.
 小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应,老师告诉同学们,高温下,铁与水蒸气能反应生产一种常见的铁的氧化物和一种气体,小杰很好奇,设计如图实验探究铁粉与水蒸气反应后的产物.
小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应,老师告诉同学们,高温下,铁与水蒸气能反应生产一种常见的铁的氧化物和一种气体,小杰很好奇,设计如图实验探究铁粉与水蒸气反应后的产物.(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是氢气.
(3)探究试管汇总剩余固体成分是什么?
【查阅资料】常见的铁的氧化物有FeO(黑色、没有磁性)、Fe2O3,Fe3O4
【初步验证】试管中固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe3O4,猜想二:剩余固体是Fe与Fe3O4
【实验探究】
| 实验操作 | 实验现象结论 |
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.
1.小组的同学在实验室将一定量的稀硫酸加入到盛有氢氧化钠溶液的烧杯中,未看到明显的现象.部分同学产生了疑问:酸和碱到底能不能发生反应?
(1)该小组同学又做了如下实验:
(2)同学们对(1)实验反应后溶液中的溶质组成展开了探究,做出如下猜想:
甲的猜想是:Na2SO4和NaOH
乙的猜想是:Na2SO4
你的猜想是:Na2SO4和H2SO4
你认为甲的猜想不合理.理由是溶液变为了无色,说明不含有氢氧化钠.
若要验证余下的两种猜想,请完成下面的实验方案.
(1)该小组同学又做了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 向底油酚酞溶液的稀氢氧化钠溶液的试管中,加入稀硫酸并振荡 | 观察到溶液由 红色变为无色 | 氢氧化钠和稀硫酸发生看反应,方程式 H2SO4+2NaOH═Na2SO4+2H2O |
甲的猜想是:Na2SO4和NaOH
乙的猜想是:Na2SO4
你的猜想是:Na2SO4和H2SO4
你认为甲的猜想不合理.理由是溶液变为了无色,说明不含有氢氧化钠.
若要验证余下的两种猜想,请完成下面的实验方案.
| 实验步骤 | 预期实验现象 | 实验结论 |
| 取(1)试验后溶液少量于试管中,加入锌或碳酸钙 (用两种不同类别的物质) | 生成气泡 或没有气泡产生 | 你的猜想正确 |
2.下列排顺不正确的是( )
| A. | 地壳中元素含量: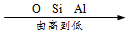 | B. | 物质的溶解性: | C. | 铁元素质量分数: | D. | 金属的活动性: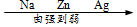 |
